Snáď každá domáca kuchyňa má sódu -neopísateľný box s práškovou hmotou. Gazdinky ho používajú ako kulinársku pomôcku pri pečení. Rozsah jeho aplikácie je však taký široký, že látku možno sebavedomo nazvať univerzálnym ľudským asistentom. Ale čo je to vlastne sóda? V akých formách existuje a ako sa používa v každodennom živote?

Názvy sódy
Predtým, ako prejdeme k chemickým vlastnostiam sódy,stojí za zmienku, že jeho názov - „sóda“, látka získaná z názvu rastlinného sódy, ktorého popol bol zdrojom extrakcie sódy.
V chémii je sóda generický názov pre sodné soli kyseliny uhličitej:
- Na2CO3 (uhličitan sodný) - chemický vzorec sódy;
- Na2CO310H2O - sóda bikarbóna;
- NaHCO3 - prášok na pečenie. Toto je chemický vzorec sódy bikarbóny;
- Na2CO3H2O alebo Na2CO37H2O je chemický vzorec kryštalickej sódy.
V každodennom živote, ako aj v chemickom priemysle existuje pre látku niekoľko triviálnych názvov:
- prášok na pečenie;
- prášok na pečenie;
- hydrogenuhličitan sodný;
- prísada E500;
- dekahydrát sodný.

Empirický vzorec
Chemický vzorec sódy bikarbóny - NaHCO3... Je to kyslá soľ kyseliny uhličitej. Ak spočítate atómové hmotnosti všetkých jeho prvkov, získate atómovú hmotnosť sódy rovnajúcu sa 84 amu. e.
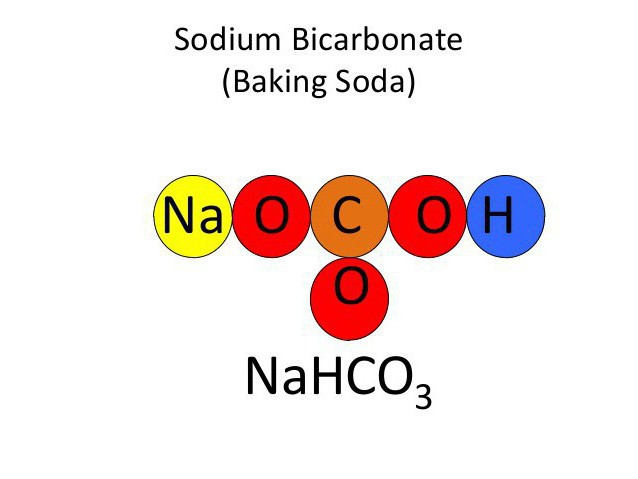
Spôsob jeho vzniku je veľmi jednoduchý. Chemický vzorec sódy bikarbóny je komplexná interakcia hydroxidu sodného s kyselinou uhličitou:
NaOH + H2CO3 = NaHCO3 + H2O.
V oblasti chémie je hydrogenuhličitan sodnýkomplex katiónu sodného a aniónu bikarbonátu. Keď sa tieto prvky zavedú do tela, normalizujú acidobázickú rovnováhu a neutralizujú prebytok kyselín obsiahnutých v kvapalnom médiu.
Sóda
Chemický vzorec sódy je Na2CO3. Soda je biela, voľne tečúca látka, ktorá môže byť vo forme granúl (A) alebo prášku (B).
Tento druh sódy má množstvo funkcií, ktoré odlišujú sodu od sódy bikarbóny.
- pH prostredia. Sóda bikarbóna aj sóda sú zásadité, ale prvá je slabá s pH = 8 a druhá je silná s pH = 11. O povahe životného prostredia svedčí aj chemický vzorec technickej sódy.
- Oblasť použitia. Sóda bikarbóna sa používa v potravinárskom priemysle, kozmetike a medicíne. Kalcinovaný prášok sa používa ako účinný čistiaci prostriedok.
V domácnosti pomocou sódy môžete:
- pranie, používanie ako prací prášok;
- na umývanie podláh však tento nástroj nebude fungovať na laminát a parkety, pretože môže zničiť povlak;
- odstrániť upchatie potrubia;
- na čistenie kameninových výrobkov.
Pri použití sódy musíte byť veľmi opatrní, pretože látka je veľmi toxická a patrí do tretej skupiny nebezpečných látok.

Fyzikálne vlastnosti sódy bikarbóny
Hydrogenuhličitan sodný je biela prášková látka. Je to komplex prvkov sodíka, vodíka, uhlíka a kyslíka.
Hustota prášku je 2,16 g / cm3.

Pri teplote +50 ° Co–60oS látkou sa začína topiť.
Hydrogenuhličitan sodný alebo sóda bikarbóna sa dodáva vo forme mliečneho prášku. Dokonale sa rozpustíme vo vodnom médiu. Nehorí. Chemický vzorec sódy bikarbóny je rovnaký ako u sódy bikarbóny.
Roztok sódy

Sóda bikarbóna je látka, ktorá sa vo vode úplne rozpúšťa a vzniká roztok sódy. Na hygienické účely sa používa ako ústna voda.
Chemický vzorec roztoku sódy je nasledujúci:
NaHCO3 + H2O = H2CO3 + NaOH.
Vodný roztok sódy má mierne zásaditý charakter.
Hydrogenuhličitan sodný vo vodnom roztoku sa disociuje za vzniku nasledujúcich iónov:
Na2CO3 ↔ 2Na+ + CO32-
Vlastnosti sódy ako zásady
Ako už bolo mnohokrát spomenuté, bikarbonátsodík je zásaditá látka. Táto skutočnosť ovplyvňuje používanie sódy ako prostriedku na neutralizáciu zvýšenej kyslosti tela, najmä žalúdka. Prvky, ktoré tvoria látku, majú bezpečný účinok.
Soda zvyšuje účinnosť obličiek, pretoževylúčený moč je zásaditý. Navyše v tele zadržiava potrebné množstvo glutamínu AA, čo zabraňuje vzniku kamenných útvarov v obličkách.
Alkalické prostredie napomáha lepšej absorpcii niektorých vitamínov B: B1, B4, B5, B6 a B12.
Pri použití sódy na jej dobrú absorpciuv kombinácii s horúcim mliekom. To prispieva k tomu, že v častiach tenkého čreva sóda interaguje s aminokyselinami mlieka, v dôsledku čoho sa objavujú sodné soli aminokyselín zásaditého charakteru. Tieto aminokyseliny prenikajú do krvného obehu oveľa lepšie ako sóda bikarbóna, čím sa zvyšujú zásadité zásoby tela.
Lúh sodný
Chemický vzorec hydroxidu sodného je NaOH. Štrukturálny vzorec: Na - O - H.
Molekulová hmotnosť látky sa skladá z atómových hmotností jej zložiek Na, O a H. Je rovná 40.
Žieravina je vysoko rozpustná vo vode.
V priemysle sa pre tento druh sódy používajú nasledujúce názvy:
- hydroxid sodný;
- hydroxid sodný;
- hydrát oxidu sodného.
Pri práci s lúhom sodným je potrebné používať ochranný odev, pretože pri kontakte s pokožkou spôsobuje vážne popáleniny.
Soda v komplexe s octom
Chemický vzorec octu a sódy je kaliaca reakcia, pri ktorej vzniká voda, oxid uhličitý a soľ kyseliny octovej.

Tento chemický „experiment“ sprevádza charakteristický sykot, ktorý naznačuje začiatok „horenia“ sódy.
Táto reakcia sa vykonáva v kulinárskom obchode, keďmienite zamiesiť cesto na pečenie. Ocot sa na to odoberá v koncentrácii 9%. Analógom kyseliny môže byť citrónová šťava, jablčný ocot alebo vínny ocot.
Prečo teda vykonávať túto reakciu pri tvorbe cesta? Faktom je, že oxid uhličitý produkovaný počas rozkladu sódy dodáva cestu nádheru.
Získanie látky
Sóda bola kedysi extrahovaná z popola rastliny hodgepodgesodoniferous. V súčasnej dobe je základom pre získanie tejto látky prírodný síran sodný. Reakcia na získanie je nasledovná, kde je chemický vzorec sódy zobrazený na pravej strane:
Na2s4 + 3C + 2O2 = 2Na2CO3 + CO2 + 2 SO2;
CaCO3 + C + Na2s4 = Na2CO3 + 4CO + CaS.
Pomocou sódy bikarbóny
Soda je veľmi obľúbená v každodennom živote, a to nielen ako kulinárska zložka. Poďme sa však bližšie pozrieť na prípady, kde sa používa sóda.
- Na začiatok stojí za zmienku ešte raz, že sóda -potravinárska zložka v kulinárskom obchode. Jeho použitie nie je náhodné: keď je látka zahriata, je schopná emitovať pary oxidu uhličitého, čo zase dodáva testu vzdušnosť. V tomto prípade sóda bikarbóna funguje ako prášok do pečiva. Ak si však v obchode kúpite vrecko s cukrovinkovým práškom do pečiva, potom na obale v rade na zloženie nájdete prítomnosť sódy, ktorá je označovaná ako potravinárska prídavná látka E500.
- Sóda bikarbóna sa používa aj na výrobu sýtených nápojov.
- Veľmi často sa sóda používa v tzv"Ľudová" medicína. V tejto oblasti sóda pôsobí ako všeliek na takmer každé ochorenie, napríklad jej účinnosť bola preukázaná pri pálení záhy, kašli, bolestiach hrdla, žalúdka a zvýšenej teplote.
- Sóda bikarbóna fungovala dobre aj ako čistiaci prostriedok.prostriedky. Môže byť použitý na čistenie vodovodných zariadení, hliníkových hrncov, riadu, kobercov, striebra a na pranie odevov. Látka má dobré dezinfekčné a protiplesňové činidlo.
- Mnoho žien používa sódu bikarbónu v kozmetikea na hygienické účely. Môže byť použitý ako peeling na pokožku. Tento nástroj dokonale uvoľní drsnú pokožku chodidiel, ak sa používa na kúpele na nohy. S jeho pomocou sa môžete zbaviť zápachu potu v oblasti podpazušia aj v topánkach.
Sóda pomôže aj pri bielení zubov. Je to lacná, ale účinná metóda. Sódový prášok sa zmieša so zubnou pastou alebo vodou a zuby sa čistia jemnými pohybmi.
Lúh sodný: aplikácia
Použitie tohto druhu sódy musí sprevádzať určité bezpečnostné opatrenia, pretože lúh sodný je silná zásada, ktorá môže „korodovať“ mnoho typov povrchov.
Na čo môže byť leptadlo užitočné v domácom prostredí?
- Žieravina robí vynikajúcu prácu s rôznymišpina na riade. Mali by ste sa však zdržať používania tohto nástroja na výrobky z hliníka a teflónu. Ale pre ostatné hrnce, panvice alebo podnosy - prosím. Usadeniny uhlíka, vodný kameň, zatuchnuté vrstvy tuku - lúh sodný sa s tým všetkým ľahko vyrovnajú.
- Lúh sodný môže vyriešiť problém s upchatým potrubím. Musíte len naliať granulovanú látku do potrubia a nechať ju chvíľu pôsobiť, potom ju opláchnuť tečúcou vodou.
Lúh sodný, známy tiež ako lúh sodný, sa na priemyselnej úrovni široko používa v rôznych oblastiach výroby.
- V stavebníctve. Tu sa látka používa na výrobu niektorých typov stavebných materiálov a slúži aj ako ďalší komponent, ktorý posilňuje základný základ štruktúr.
- V potravinárskom priemysle.Lúh sodný je tiež užitočný pri výrobe potravín. V tomto prípade sa samozrejme používa v nízkej koncentrácii. S jeho účasťou sa vyrábajú kakaové prášky a čokoláda, zmrzlina, karamelky, pri pečení chleba, používa sa ako prísada do E524.
- Textilný priemysel. V tejto oblasti je lúh sodný užitočný na bielenie tkanín a regeneráciu gumových výrobkov.
- Chemická výroba:Lúh sodný sa používa ako neutralizátor kyselín, prostriedok na čistenie oleja a výrobkov na jeho základe. Výroba technických olejov tiež nie je úplná bez pridania hydroxidu sodného. Lúh sodný je navyše dobrým katalyzátorom niektorých chemických reakcií.
- Lúh sodný je tiež použiteľný na výrobu mydla pri výrobe rôznych typov mydiel, šampónov a gélov.
Sóda: použite
Sóda sa nazýva aj bielizeň. Tento nástroj bol obzvlášť žiadaný dokonca aj v Sovietskom zväze, preto možno tvrdiť: ľanová sóda bola testovaná časom.
Nástroj sa používa v nasledujúcich situáciách:
- Pri umývaní vecí.
- Pri čistení povrchov dlaždíc, keramiky, fajansy.
- Pri odstraňovaní upchatia potrubí.
- Na odstránenie vodného kameňa v bubnoch práčky, ako aj na riade.
- Na ničenie škodlivého hmyzu v zeleninových záhradách.
Z vyššie uvedeného vyplýva záver: sóda je univerzálnym prostriedkom, ktorý sa používa vo väčšine oblastí života v domácnosti i v priemysle.
Pozitívnou kvalitou látky je, že sa dá kúpiť za pouhých penny.




