V periodické tabulce Mendělejeva na čísle 1nachází se nejběžnější prvek ve vesmíru - vodík. Jeho distribuce se v procentech blíží 75%. Jeho nejnižší obsah je zaznamenán ve vrstvách atmosféry - 0,0001%. Zemská kůra obsahuje 1% hmotnosti plynu. Jeho největší množství se nachází ve vodě: 12%. Jedná se o třetí nejrozšířenější chemický prvek na naší planetě.
Popis položky
Molekula vodíku, jejíž vzorec je H-H nebo H2, má fyzikální a chemické vlastnosti.

Vodík je plyn, který není vybaven ani jednímbarva, žádný zápach. Umístění vodíku v tabulce na 1. místě je dáno skutečností, že za různých podmínek se tento prvek může projevovat jako kov nebo jako plyn. Ve svém vnějším orbitálu je 1 elektron, který může vodík dát (kovové vlastnosti) nebo jiný (kvalita plynu).
Průměr molekuly vodíku je 27 nm.
Průměr atomu vodíku je 1A, poloměr 0,41 A.
Vlastnosti
Fyzické zahrnují následující:
- Bod varu - 256oC.
- Teplota tání -259,2oC.
- Hmotnost vzduchu (D) - 0,069.
- Vodík je ve vodě špatně rozpustný.
Chemické vlastnosti jsou následující:
- Nepolární vazba mezi částicemi molekuly má energii 436 kJ / mol.
- Teplota tepelné disociace je 2000oC.
- Reaguje s:
- halogeny;
- kyslík;
- šedá;
- dusík;
- oxid dusnatý;
- aktivní kovy.
V přírodních podmínkách se vodík vyskytuje jak přirozeně, tak ve formě izotopů: protium, deuterium a tritium.
Struktura molekuly
Molekula prvku má jednoduchou strukturu.Složení molekuly vodíku je reprezentováno dvěma atomy, které se blíží a tvoří kovalentní nepolární vazbu a také jeden elektronový pár. Struktura jednoho atomu je: 1 pozitivně nabité jádro, kolem kterého se pohybuje 1 negativně nabitý elektron. Tento elektron se nachází na orbitálu 1 s.
H - 1e = H + tento vodíkový ion je pozitivní.
Tento výraz naznačuje, že vodíkmá podobné parametry jako prvky skupiny 1 v periodickém systému, kterými jsou alkalické kovy (lithium, sodík, draslík), darující svůj jediný elektron na vnějším orbitálu.
Н + 1е = Н– negativní iont vodíku.
Tato rovnice ukazuje, že vodík jesouvisející s podobnými prvky ze 7. skupiny, kterými jsou plyn a jsou schopné přijímat chybějící elektrony na svoji vnější elektronickou úroveň. Mezi tyto plyny patří fluor, chlor, brom atd.
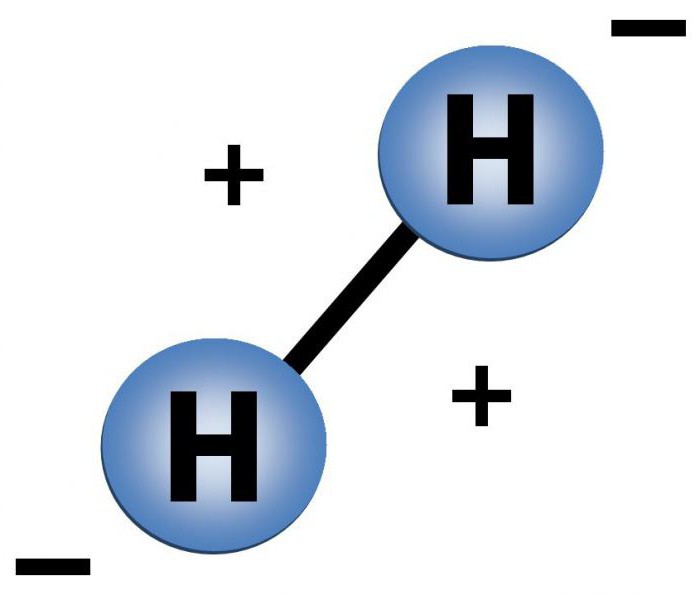
Složení molekuly vodíku je graficky znázorněno níže.

Vzdálenost mezi atomy vodíku r = 0,74 A, czatímco součet orbitálních poloměrů je 1,06 A. To ovlivňuje hloubku překrytí elektronových mraků a silnou, stabilní vodíkovou vazbu.
Atom vodíku je nejelementárnějším atomem v přírodě. Velikost atomového protonu je 10,5 A a průměr jednoho atomu je 0,1 nm.
Molekuly izotopů mají zvláštní strukturu. Atomové jádro protia se skládá pouze z jednoho protonu. Izotop je označen: 1H.
Jaderná struktura vypadá jako komplex protonu a neutronu (2H).
3H - tritium - ve své atomové struktuře je vybaveno jádrem s 1 protonem a dvěma neutrony.
Hmotnost
Ve vědě existují vzorce, které vypočítávají hmotnost molekuly vodíku. Ve vztahu k prvku jsou určeny molekulové a atomové hmotnosti.

Molární hmotnost molekuly vodíku se vypočítá podle obecného vzorce:
M = m / n, kde m je hmotnost látky, n je její množství.
Hmotnost atomu je 1,008 amu.Relativní hmotnost molekuly bude tedy rovna 1,008. Protože molekula vodíku se skládá ze dvou atomů, relativní atomová hmotnost je 2,016 amu. e. m. Hmotnost molekuly vodíku je vyjádřena v gramech na mol (g / mol).
Hodnota v přírodě

Nejvýznamnější přírodní látkou, která v komplexu s kyslíkem tvoří vodík, je voda. Voda je zdrojem života, proto je vodík životně důležitým prvkem.
Ze 100% všech chemických prvků, kterétvoří organické prostředí, 1/10 dílu, neboli 10%, je vodík. Kromě vody je schopen udržovat kvartérní proteinovou strukturu, což je možné díky vodíkové vazbě.
Princip komplementarity nukleových kyselinnastává také působením molekuly vodíku. V rostlinné buňce se H účastní procesu fotosyntézy, biosyntézy a přenosu energie membránovými kanály.
přihláška
Vodík je široce používán v chemickém průmyslu. Přidává se při výrobě plastových výrobků, při výrobě mýdla, stejně jako při výrobě čpavku a mentolu.
Potravinářský průmysl:při výrobě potravin se vodík přidává jako potravinářská přídatná látka E949. Taková složka je vidět na obalu margarínu, rostlinných olejů. Aditivum E949 je schváleno potravinářským průmyslem Ruské federace.
Vodík byl kdysi používán vletecký průmysl, protože látka je lehčí než vzduch. Takže ve 30. letech minulého století byly balóny a vzducholodě naplněny tímto typem plynu. Navzdory své lacnosti a snadnému použití se vodík brzy přestal používat jako plnivo, protože případy leteckých výbuchů byly stále častější.
V současné době se plyn používá jako palivo,používané v kosmickém průmyslu. Zvažují se však způsoby jeho použití pro provoz motorů osobních a nákladních automobilů, protože prvek během spalování nevypouští škodlivé nečistoty do atmosféry, a proto je šetrný k životnímu prostředí.
Nedílnou součástí izotopů vodíkupůsobí jako součást mnoha léků. Deuterium se používá ve farmakologickém výzkumu ke stanovení chování a účinků léčiva v těle. Tritium se používá v radiodiagnostice jako prvek, který určuje biochemické reakce metabolismu enzymů. Vodík je součástí peroxidu, který je dezinfekčním prostředkem.






