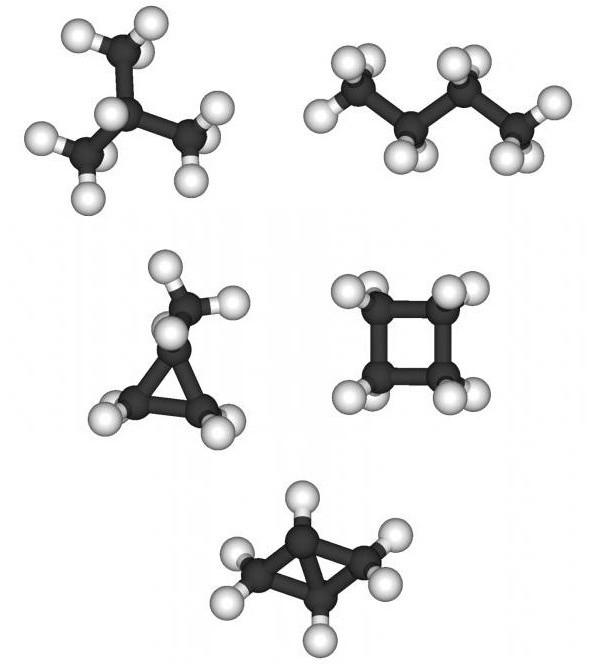
Os hidrocarbonetos são a classe mais simples de orgânicossubstâncias, suas moléculas têm átomos de apenas dois elementos químicos - carbono e hidrogênio. A maioria das classes de compostos orgânicos são obtidas a partir de vários hidrocarbonetos usando métodos de síntese química.
Os hidrocarbonetos são divididos em duas subclasses -acíclico e cíclico. Os seguintes grupos pertencem a hidrocarbonetos acíclicos, ou hidrocarbonetos graxos, ou hidrocarbonetos alifáticos: hidrocarbonetos saturados (alcanos), insaturados (alcenos, alcinos, dienos), terpenos acíclicos. Os hidrocarbonetos cíclicos são representados por grupos cicloparafinas, arenos e terpenos cíclicos. Às vezes, os terpenos são classificados como objetos de estudo em química bioorgânica.
Hidrocarbonetos saturados (alcanos) - compostoscarbono e hidrogênio, em cujas moléculas todas as valências remanescentes após a conexão dos átomos de carbono por uma simples ligação estão saturadas de átomos de hidrogênio. Todos os alcanos podem ser considerados derivados ou homólogos do metano. Se um átomo de hidrogênio é removido do metano, que tem a fórmula molecular CH4, uma partícula é formada - o radical CH3. Pelo fato de o olerode ser geralmente tetravalente em uma molécula de substância orgânica, a combinação de dois desses radicais ocasiona o surgimento do segundo representante da série homóloga - o etano (C2H6). Se um átomo de hidrogênio é subtraído do etano, forma-se um radical etil que, após se combinar com o CH3, forma um terceiro homólogo, o propano.
Ao analisar a fórmula estrutural do propano, é fácilpara estabelecer que sua molécula inclui dois tipos de átomos de carbono - primários e secundários. Cada átomo de carbono primário está ligado a um átomo de carbono por uma de suas valências, e o secundário - por duas valências com dois átomos de carbono. Se você subtrair o átomo de hidrogênio do átomo de carbono primário do propano, o propil primário é formado, a partir do secundário - propil secundário. A ligação ao corte primário ou secundário de metil causa a formação de variedades estruturais do quarto homólogo. Dois compostos são formados, butano normal de cadeia linear e isobutano de cadeia ramificada.
Hidrocarbonetos saturados: estrutura
O metano é um representante típico dos alcanos.Fórmula molecular CH4. As moléculas de alcano são caracterizadas por uma ligação sigma. Em uma molécula de metano, um átomo de carbono forma quatro ligações covalentes devido a um orbital s e três orbitais p, e cada átomo de hidrogênio - devido a um orbital s.
Hidrocarbonetos saturados: nomenclatura e isomerismo
Ao derivar as fórmulas estruturais do homólogouma série de metano, começando com butano C4H10, encontramos o fenômeno de isomerismo. Por exemplo, a fórmula molecular C4H10 corresponde a dois compostos individuais, C5H12 - três. Posteriormente, o número de isômeros aumenta com o número de átomos de carbono na molécula de alcano. Por exemplo, a fórmula molecular C6H14 corresponde a cinco fórmulas estruturais e, consequentemente, substâncias individuais, C7H16 - 9, C8H18 - 18, C10H22 - 76, C12H26 - 355. Os primeiros quatro representantes de alcanos são gases, do quinto ao décimo segundo - líquidos, a partir do décimo sexto - sólidos ...
Propriedades químicas de hidrocarbonetos saturados
Todos os hidrocarbonetos saturados são substâncias inertes.Isso se deve ao fato de que nas moléculas de alcano, os átomos de carbono e hidrogênio estão ligados por ligações sigma, de modo que esses compostos não podem anexar átomos de hidrogênio. Alcanos entram em reações de halogenação, nitração e clivagem radical. No processo de halogenação, os átomos de halogênio substituem facilmente os átomos de hidrogênio na molécula de alcano. Durante a nitração, o grupo nitro substitui facilmente o hidrogênio no terciário, mais difícil - nos átomos de carbono secundários e primários.
Hidrocarbonetos saturados e insaturados sãomatéria-prima para a obtenção de diversas substâncias orgânicas. Separando os átomos de hidrogênio dos hidrocarbonetos saturados, os insaturados (alcenos, alcinos) podem ser obtidos.