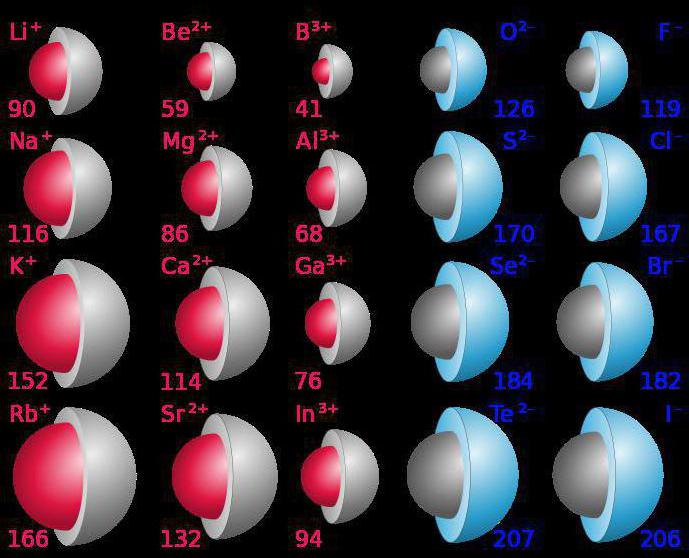
Makrocząsteczka to cząsteczka, która mawysoka masa cząsteczkowa. Jego struktura jest przedstawiona w postaci wielokrotnie powtarzających się linków. Rozważmy cechy takich związków, ich znaczenie dla życia żywych istot.
Cechy kompozycji
Biologiczne makrocząsteczki powstają z setek tysięcy małych materiałów wyjściowych. Żywe organizmy charakteryzują się trzema głównymi typami makrocząsteczek: białkami, polisacharydami, kwasami nukleinowymi.
Ich początkowe monomery tomonosacharydy, nukleotydy, aminokwasy. Makrocząsteczka stanowi prawie 90 procent masy komórek. W zależności od sekwencji reszt aminokwasowych powstaje specyficzna cząsteczka białka.
Substancje o masie molowej powyżej 103 Da są uważane za substancje o dużej masie cząsteczkowej.

Historia tego terminu
Kiedy pojawiła się makrocząsteczka? Koncepcja ta została wprowadzona przez laureata Nagrody Nobla w dziedzinie chemii Hermanna Staudingera w 1922 roku.
Cewkę polimerową można postrzegać jakosplątana przędza spowodowana przypadkowym rozwinięciem szpuli w całym pomieszczeniu. Ta cewka systematycznie zmienia swoją konformację; to jest przestrzenna konfiguracja makrocząsteczki. Jest podobny do trajektorii ruchu Browna.
Powstawanie takiej plątaniny następuje z powoduże w pewnej odległości łańcuch polimeru „traci” informację o kierunku. O cewce można mówić, gdy długość związków wielkocząsteczkowych jest znacznie większa niż długość fragmentu strukturalnego.
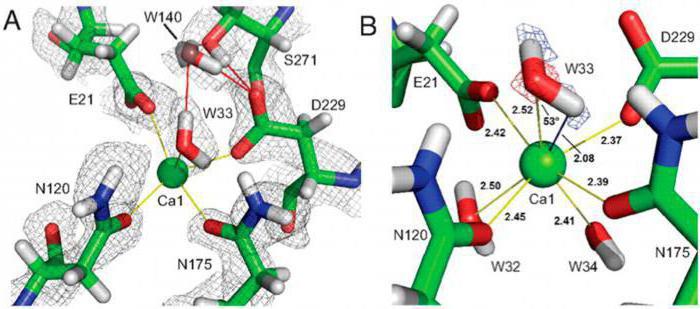
Konfiguracja kulista
Makrocząsteczka to gęsta konformacja, wktóry można porównać ułamek objętościowy polimeru z jednostką. Stan globularny jest realizowany w tych przypadkach, gdy występuje wzajemne przyciąganie się przy wzajemnym działaniu poszczególnych jednostek polimeru między sobą a środowiskiem zewnętrznym.
Replika struktury makrocząsteczki to część wody, która jest włączona jako element takiej struktury. Jest to najbliższe uwodnione środowisko makrocząsteczki.

Charakterystyka cząsteczki białka
Makrocząsteczki białka są hydrofiloweSubstancje. Gdy suche białko rozpuszcza się w wodzie, początkowo pęcznieje, a następnie obserwuje się stopniowe przejście w roztwór. Podczas pęcznienia cząsteczki wody wnikają w białko i wiążą jego strukturę grupami polarnymi. Jednocześnie rozluźnia się gęste upakowanie łańcucha polipeptydowego. Spuchnięta cząsteczka białka jest uważana za rozwiązanie odwrotne. Wraz z późniejszą absorpcją cząsteczek wody obserwuje się oddzielenie cząsteczek białka od całkowitej masy, a także zachodzi proces rozpuszczania.
Ale pęcznienie cząsteczki białka nie we wszystkich przypadkach powoduje rozpuszczenie. Na przykład kolagen po wchłonięciu cząsteczek wody pozostaje w stanie spęcznienia.

Teoria nawodnienia
Zgodnie z tą teorią związki o dużej masie cząsteczkowej nie sąpo prostu adsorbują, następuje elektrostatyczne wiązanie cząsteczek wody z polarnymi fragmentami rodników bocznych aminokwasów, które mają ładunek ujemny, a także aminokwasów zasadowych, które mają ładunek dodatni.
Woda częściowo uwodniona jest związana grupami peptydowymi, które tworzą wiązania wodorowe z cząsteczkami wody.
Na przykład polipeptydy, które mająniepolarne grupy boczne. Po połączeniu z grupami peptydów odpycha łańcuchy polipeptydowe od siebie. Obecność mostków międzyłańcuchowych nie pozwala na całkowite odłączenie cząsteczek białka i przeniesienie ich do postaci roztworu.
Struktura makrocząsteczek jest niszczona przez ogrzewanie, co powoduje pękanie i uwalnianie łańcuchów polipeptydowych.

Właściwości żelatyny
Żelatyna ma podobny skład chemiczny do kolagenu, z wodą tworzy lepką ciecz. Jedną z charakterystycznych właściwości żelatyny jest jej zdolność żelowania.
Tego typu cząsteczki są używane jako substytuty hemostatyczne i osocze. Zdolność żelatyny do tworzenia żeli wykorzystywana jest do produkcji kapsułek w przemyśle farmaceutycznym.
Cecha rozpuszczalności makrocząsteczek
Te typy cząsteczek mają różnerozpuszczalność w wodzie. Decyduje o tym skład aminokwasów. W obecności w strukturze aminokwasów polarnych zdolność do rozpuszczania się w wodzie znacznie wzrasta.
Cecha ma również wpływ na tę właściwośćorganizacja makrocząsteczki. Białka globularne mają wyższą rozpuszczalność niż makrocząsteczki włókniste. W trakcie licznych eksperymentów ustalono zależność rozpuszczania od właściwości zastosowanego rozpuszczalnika.
Podstawowa struktura każdej cząsteczki białka jest inna, co nadaje białku indywidualne właściwości. Sieciowanie między łańcuchami polipeptydowymi zmniejsza rozpuszczalność.
Pierwotna struktura cząsteczek białka powstaje dzięki wiązaniom peptydowym (amidowym), gdy ulega zniszczeniu, następuje denaturacja białka.
Wysalanie
Aby zwiększyć rozpuszczalność cząsteczek białkaużywaj roztworów soli obojętnych. Na przykład w podobny sposób można przeprowadzić selektywne wytrącanie białek, przeprowadzić ich frakcjonowanie. Liczba otrzymanych cząsteczek zależy od początkowego składu mieszaniny.
Osobliwością białek, które uzyskuje się przez wysalanie, jest zachowanie właściwości biologicznych po całkowitym usunięciu soli.
Istotą procesu jest usuwanie anionów ikationy soli uwodnionej otoczki białkowej, co zapewnia stabilność makrocząsteczki. Maksymalna liczba cząsteczek białka jest wysalana przy użyciu siarczanów. Metoda ta służy do oczyszczania i separacji makrocząsteczek białek, ponieważ różnią się one znacznie wartością ładunku, parametrami powłoki hydratacyjnej. Każde białko ma własną strefę wysalania, to znaczy należy dobrać do niego sól o danym stężeniu.

Aminokwasy
Obecnie znanych jest około dwustu aminokwasów, które są częścią cząsteczek białek. W zależności od struktury dzielą się na dwie grupy:
- proteinogenne, które są częścią makrocząsteczek;
- nieproteogenny, nie biorący czynnego udziału w tworzeniu białek.
Naukowcom udało się rozszyfrować sekwencjęaminokwasy w wielu cząsteczkach białek pochodzenia zwierzęcego i roślinnego. Wśród aminokwasów, które dość często występują w składzie cząsteczek białka, wyróżniamy serynę, glicynę, leucynę, alaninę. Każdy naturalny biopolimer ma swój własny skład aminokwasów. Na przykład protaminy zawierają około 85 procent argininy, ale nie są to kwasowe, cykliczne aminokwasy. Fibroina to cząsteczka naturalnego białka jedwabiu, która zawiera około połowy glicyny. Kolagen zawiera tak rzadkie aminokwasy, jak hydroksyprolina, hydroksylizyna, których nie ma w innych makrocząsteczkach białek.
Skład aminokwasów zależy nie tylko od właściwości aminokwasów, ale także od funkcji, przeznaczenia makrocząsteczek białek. O ich kolejności decyduje kod genetyczny.
Poziomy organizacji strukturalnej biopolimerów
Istnieją cztery poziomy: podstawowy, drugorzędny, trzeciorzędny i czwartorzędowy. Każda konstrukcja ma swoje własne charakterystyczne cechy.
Podstawową strukturą cząsteczek białka jest liniowy łańcuch polipeptydowy z reszt aminokwasowych połączonych wiązaniami peptydowymi.
To właśnie ta struktura jest najbardziej stabilna, ponieważ zawiera wiązania kowalencyjne peptydów między grupą karboksylową jednego aminokwasu a grupą aminową innej cząsteczki.
Struktura drugorzędowa obejmuje zwijanie łańcucha polipeptydowego za pomocą wiązań wodorowych w postaci helikalnej.
Trzeciorzędowy typ biopolimeru uzyskuje się przez przestrzenne pofałdowanie polipeptydu. Spiralne i warstwowo złożone formy struktur trzeciorzędowych są podzielone.
Białka globularne charakteryzują się eliptycznym kształtem, natomiast cząsteczki fibrylarne - wydłużonym.
Jeśli makrocząsteczka zawiera tylko jeden plikłańcuch polipeptydowy, białko ma tylko strukturę trzeciorzędową. Na przykład jest to białko tkanki mięśniowej (mioglobina), które jest wymagane do wiązania tlenu. Niektóre biopolimery są zbudowane z kilku łańcuchów polipeptydowych, z których każdy ma strukturę trzeciorzędową. W tym przypadku makrocząsteczka ma strukturę czwartorzędową, składającą się z kilku globul połączonych w dużą strukturę. Hemoglobinę można uznać za jedyne czwartorzędowe białko zawierające około 8 procent histydyny. To on jest aktywnym buforem wewnątrzkomórkowym w erytrocytach, który pozwala na utrzymanie pH krwi na stabilnym poziomie.
Kwasy nukleinowe
Są to związki o dużej masie cząsteczkowejktóre są tworzone przez fragmenty nukleotydów. RNA i DNA znajdują się we wszystkich żywych komórkach, to one pełnią funkcję przechowywania, przekazywania, a także uświadamiania sobie informacji dziedzicznych. Monomery to nukleotydy. Każdy z nich zawiera pozostałą część zasady azotowej, węglowodanów i kwasu fosforowego. Badania wykazały, że zasada komplementarności jest obserwowana w DNA różnych organizmów żywych. Kwasy nukleinowe są rozpuszczalne w wodzie, ale nierozpuszczalne w rozpuszczalnikach organicznych. Te biopolimery są niszczone, gdy wzrasta temperatura, promieniowanie ultrafioletowe.
Zamiast kończyć
Oprócz różnych białek i kwasów nukleinowych,makrocząsteczki to węglowodany. Polisacharydy mają w swoim składzie setki monomerów, które mają przyjemny słodkawy smak. Jako przykłady hierarchicznej struktury makrocząsteczek można przytoczyć ogromne cząsteczki białek i kwasów nukleinowych ze złożonymi podjednostkami.
Na przykład przestrzenna struktura kulistejcząsteczka białka jest konsekwencją hierarchicznej wielopoziomowej organizacji aminokwasów. Pomiędzy poszczególnymi poziomami istnieje ścisłe powiązanie, elementy wyższego poziomu są połączone z niższymi warstwami.
Wszystkie biopolimery pełnią ważną i podobną funkcję.Stanowią budulec żywych komórek i są odpowiedzialne za przechowywanie i przekazywanie informacji dziedzicznych. Każda żywa istota charakteryzuje się specyficznymi białkami, dlatego biochemicy stają przed trudnym i odpowiedzialnym zadaniem, którego rozwiązanie ratują żywe organizmy przed pewną śmiercią.