В химии существуют группы органических веществ, różniące się podobnymi właściwościami i połączone ogólnym wzorem, który opisuje regularność różnicy strukturalnej między każdym kolejnym członkiem grupy od poprzedniego. Na przykład homologiczne serie alkanów, alkenów, alkinów lub innych grup. Ta nomenklatura ma ogromne znaczenie dla badań, prognozowania lub praktycznego zastosowania. W przypadku substancji organicznych połączonych w grupę obserwuje się regularne zmiany właściwości chemicznych i fizycznych, a wszystkie one korelują ze zmianą masy cząsteczkowej.
Równie ważne są zasady opisujące, jakwłaściwości substancji w przejściu z jednej grupy do drugiej. Aby zrozumieć, czym jest seria homologiczna, należy rozważyć konkretne przykłady. Dowolna grupa związków charakteryzuje się wzrostem temperatur topnienia (krystalizacji), wrzenia (kondensacji) i gęstości wraz ze wzrostem masy cząsteczkowej i liczby atomów węgla w cząsteczce.
Węglowodory nasycone nazywane są nasyconymi lubparafinowy; są to związki acykliczne (bez cykli) o normalnej lub rozgałęzionej strukturze, których atomy w cząsteczkach są połączone wiązaniami pojedynczymi. Ogólny wzór ma postać CnH2n + 2 i opisuje homologiczną serię alkanów. Cząsteczka każdego kolejnego członka zwiększa się w porównaniu z poprzednim o jeden atom C i dwa atomy H. Węglowodory nasycone obejmują:
- metan;
- etan;
- propan i tak dalej.
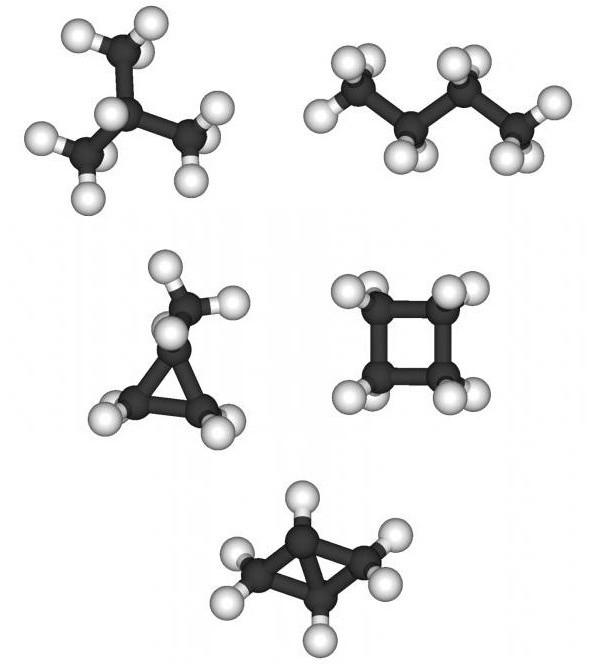
Węglowodory nasycone obejmują równieżcykloparafiny. To duża grupa związków organicznych, których cząsteczki są zamknięte w pierścieniach. Ich serie homologiczne mają wzór CnH2n, zaczynając od substancji chemicznej z trzema atomami węgla. Przykłady cykloparafin:
- cyklopropan;
- cyklobutan;
- cyklopentan i tak dalej
Węglowodory nienasycone lub nienasyconesą acykliczne. Należą do nich substancje normalne i izostrukturalne. Homologiczna seria alkenów ma ogólny wzór CnH2n. Związki te wyróżnia obecność jednego podwójnego wiązania między dwoma atomami węgla. Jeśli poprzedni rząd zaczynał się od węglowodoru z jednym atomem węgla (metan), to ten zaczyna się od substancji, której cząsteczka zawiera dwa atomy węgla. Przykłady alkenów:
- eten;
- propen;
- buten i tak dalej.
Węglowodory z dwoma atomami w cząsteczcewęgiel połączony potrójnym wiązaniem są jeszcze bardziej nienasycone, inaczej nazywa się je acetylenowymi. Są połączone homologiczną serią alkinów. Opisana jest wzorem CnH2n-2 i zaczyna się od acetylenu, który ma dwa atomy C we wzorze. Przykłady alkinów:
- etyka;
- propyn;
- butin-1 i tak dalej.
Ненасыщенные ациклические углеводороды, в cząsteczka, w której występują dwa wiązania podwójne, nazywa się dienem. Mają ogólny wzór CnH2n-2. Ich homologiczna seria zaczyna się od węglowodoru z trzema atomami węgla w cząsteczce. Wiązania podwójne mogą być sprzężone (oddzielone pojedynczym wiązaniem), kumulowane (zlokalizowane na sąsiednich atomach) lub izolowane (oddzielone kilkoma pojedynczymi wiązaniami). Przykłady dienów:
- 1,2-propadien;
- 1,3-butadien;
- izopren i tak dalej
Specjalną grupę tworzą chemikaliastruktura cykliczna, w cząsteczce której znajduje się pierścień benzenowy. Homologiczna seria najprostszych węglowodorów aromatycznych zaczyna się od związku o sześciu atomach węgla - benzenie. Homologi tej serii powstają, gdy jeden lub więcej atomów wodoru przyłączonych do pierścienia benzenowego jest zastąpionych rodnikami. W ten sposób uzyskuje się szereg substancji: benzen, toluen, ksylen. Jeśli w cząsteczce są dwa lub więcej podstawników, mówimy o obecności izomerów tych substancji. Inne homologiczne serie związków aromatycznych pochodzą z naftalenu, antracenu i innych substancji.
Jeśli w cząsteczce węglowodoru znajduje się grupa funkcyjna, to takie związki chemiczne również tworzą szereg homologiczny.
- Wiele alkoholi wyróżnia się obecnością w cząsteczcegrupa hydroksylowa (-OH). W przypadku alkoholi jednowodorotlenowych jeden atom wodoru w węglowodorze acyklicznym jest zastąpiony grupą hydroksylową; ich wzór: CnH2n + 1OH. Istnieje również szereg alkoholi wielowodorotlenowych.
- Szereg fenoli charakteryzuje się także obecnością w cząsteczce grupy hydroksylowej (-OH), ale zastępuje ona wodór w pierścieniu benzenowym.
- Wiele aldehydów wyróżnia się obecnością w cząsteczce związku chemicznego z grupy karbonylowej (> C = O); ogólny wzór dla aldehydów: R - CH = O.
- Szereg ketonów wyróżnia się również obecnością grupy karbonylowej (> C = O), ale jeśli w aldehydach jest połączona z jednym rodnikiem, to w ketonach występują dwa rodniki węglowodorowe. Formuła ketonowa: R1 - CO - R2.
- Szereg kwasów karboksylowych różni się od innych chemikaliów grupą karboksylową, która łączy w sobie grupy karbonylową i hydroksylową. Formuła - RCOOH.
Dla każdej serii, czy to serii homologicznejaldehydy, kwasy karboksylowe (organiczne), alkohole lub inne substancje, ich właściwości będą w dużej mierze zależne od rodzaju grupy funkcyjnej i będą się naturalnie zmieniać wraz ze wzrostem masy cząsteczkowej substancji. Taka klasyfikacja szerokiej klasy związków chemicznych pomaga zrozumieć naturę i zbadać ich właściwości.