周期律表ではそのような化学元素ヒ素のように、金属と非金属の境界に位置を占めます。その活動では、それは水素と銅の間に位置しています。非金属的な性質は、彼が-3(AsH)の酸化状態を示すことができるという事実に現れています。3 - アルシン) +3の正の酸化状態を有する化合物は両性特性を有し、+ 5の程度でその酸性特性が発現される。酸化ヒ素とは何ですか?

酸化物および水酸化物
以下の酸化ヒ素が存在します。2ああ3 と2ああ5。対応する水酸化物もあります。
- メタリン酸HAsO2.
- オルト砒酸H3阿蘇3.
- メタリン酸HAsO3.
- オルトミセル酸H3阿蘇4.
- ピロム酸H4なので2ああ7.

三酸化ヒ素とは何ですか?
ヒ素は2つの酸化物を形成し、そのうちAs2ああ3 三酸化物と呼ばれます。 治療によく使われる物質ですが、完全に無害な化学物質ではありません。有機ヒ素化合物(炭素との化学結合を含む化合物)などの主な供給源である無機化合物です。 Asの多くの用途2ああ3 要素の有毒な性質のために物議を醸しています。この化合物の商品名はTrisenoxです。
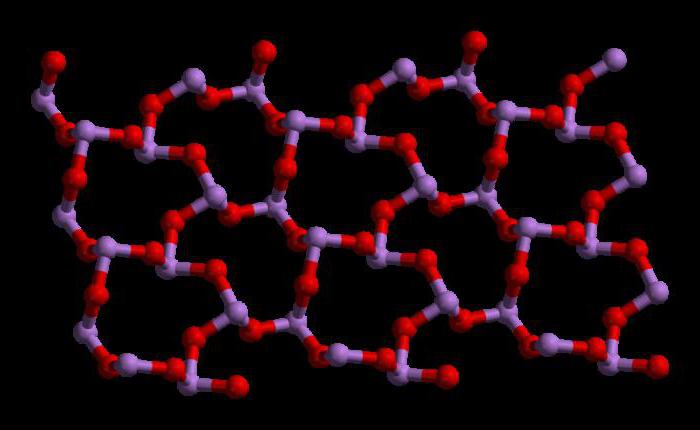
三酸化物の概要
三酸化ヒ素の化学式はAsです2ああ3..。この化合物の分子量は197.841 g / mol。この酸化物を得る方法はたくさんあります。それらの1つは硫化鉱の焙煎です。化学反応は次のとおりです。
2As2ああ3 + 9O2 →2As2ああ3 + 6SO2
ほとんどの酸化物はで得ることができます他の鉱石の処理の副産物として。アルセノパイライトは金や銅によく見られる不純物であり、空気の存在下で加熱すると三酸化ヒ素を放出します。これは深刻な中毒につながる可能性があります。

三酸化ヒ素の構造
三酸化ヒ素の式はAs4ああ6 液相および気相(800°C未満)。これらのフェーズでは、三酸化リン(P4ああ6)。しかし、800°Cを超える温度ではAs4ああ6 分子Asに分解します2ああ3..。このフェーズでは、三酸化ジイソトロン(N2ああ3)。固体状態では、この化合物は多形性能力(2つ以上の形態の結晶構造で存在する能力)を示します。
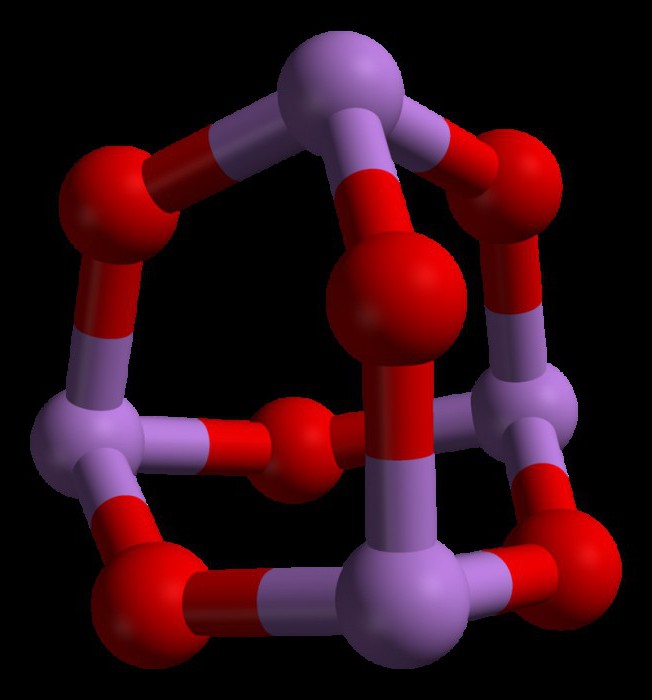
三酸化ヒ素の特性
三酸化ヒ素の主な特性のいくつかは次のとおりです。
- 三酸化物溶液は水と弱酸を形成します。これは、化合物が両性砒素酸化物であるという事実によるものです。
- それはアルカリ性溶液に可溶であり、ヒ酸塩を与える。
- 三酸化ヒ素は塩酸(HCl)への溶解度が高く、最終的に三塩化ヒ素と濃酸を生成します。
- それは五酸化物を与える(として2ああ5)過酸化水素、オゾン、硝酸などの強力な酸化剤の存在下。
- 有機溶剤にはほとんど溶けません。
- 通常の物理的状態では白い固体のように見えます。
- 融点は312.2°C、沸点は465°Cです。
- この物質の密度は4.15g / cmです。3.
医学における三酸化ヒ素の使用
この化学物質はクラスに属しています抗腫瘍薬であり、癌の治療に使用されます。ヒ素の毒性はよく知られています。しかし、三酸化ヒ素は化学薬品であり、特定の癌の治療に長年使用されてきました。この処理に使用されるソリューションは、ファウラーのソリューションと呼ばれます。 1878年、ボストン市立病院は、このソリューションがヒトの白血球数を減らすのに効果的である可能性があると報告しました。
結果として、2ああ3 主に治療に使用されました放射線療法に取って代わられるまでの白血病。しかし、1930年代以降、現代の化学療法が登場するまで、白血病の治療で徐々に人気を取り戻しました。この酸化ヒ素は、慢性骨髄性白血病の最良の治療法と考えられていました。今日でも、この物質は、レチノイドまたはアントラサイクリン化学療法の失敗を伴う特定のタイプの急性前骨髄球性白血病の治療に使用されています。また、慢性骨髄性白血病、多発性骨髄腫、急性骨髄性白血病、リンパ腫、リンパ癌の治療にも使用されます。

三酸化物の使用
三酸化ヒ素はで広く使用されています無色ガラスの製造。この化合物は、半導体や一部の合金を製造するための電子機器の分野でも有用です。塗料にも使用されています。三酸化ヒ素は脳腫瘍の効果的な治療法かもしれません。
過去にこの物質は歯科で使用されていましたが、毒性の高い化合物であるため、現代の歯科医によって使用が中止されました。酸化ヒ素(式As2ああ3)は木材防腐剤としても使用されていますが、そのような材料は世界の多くの地域で禁止されています。酢酸銅と組み合わせると、三酸化ヒ素は明るい緑色の色素を生成します。
毒性の高い物質
三酸化物自体は高レベルです毒性。したがって、使用する前に必ず必要な注意を払う必要があります。次の場合は非常に危険です。
- 食物摂取。としての場合2ああ3 誤って消化管に入った場合、すぐに医師に相談してください。医師の診察を受ける前に嘔吐を誘発することはお勧めしません。タイトな服を脱ぎ、ネクタイを外し、襟やベルトなどを開く必要があります。
- 皮膚接触。体の表面に触れた場合は、すぐに患部をたっぷりの水で洗い流してください。汚染された衣類や靴はすぐに取り除き、再利用する前に洗う必要があります。深刻な皮膚接触の場合は、直ちに医師の診察を受ける必要があります。感染部位を消毒石鹸で洗い、抗菌クリームを塗ると役立つ場合があります。
- アイコンタクト。としての場合2ああ3 目と接触する、最初にすることコンタクトレンズをすべて取り外し、15分間大量の水で目を洗い流します。冷水を使用することをお勧めします。これと並行して、誰かが救急車を呼ぶ必要があります。
- 吸入。このガスを吸い込んだ人は、新鮮な空気のある別の場所に移動する必要があります。また、すぐに医療援助を求める必要があります。呼吸が困難な場合は、すぐに酸素を注入する必要があります。犠牲者が自分で呼吸できない場合は、人工呼吸を行う必要があります。
- この化合物は有毒である可能性があります人間への影響。三酸化ヒ素は、過剰に摂取すると致命的となることさえあります。 Asを使用する場合は、常に安全メガネと手袋を着用する必要があります。2ああ3..。作業は常に換気の良い場所で行う必要があります。

副作用
この物質の一般的な副作用には、次のような症状があります。
- 食欲不振;
- 嘔吐;
- 吐き気;
- 腹痛
- 便秘;
- 頭痛;
- 倦怠感;
- めまい
- 熱;
- 呼吸の問題;
- 高い白血球数;
- 高血糖;
- 皮膚の発疹。
あまり一般的ではない副作用は次のとおりです。
- 口渇;
- 呼吸困難;
- 胸痛;
- 白血細胞数が少ない;
- 筋肉と骨の痛み;
- 顔と目の腫れ;
- 下痢;
- 身震い;
- 低血糖;
- 血中酸素濃度が低い。
副作用としてまれ2ああ3:
- 不規則な心拍(これは死に至ることさえあります);
- 体重の増加;
- 失神;
- 気晴らし;
- 昏睡;
- 腫れた腹;
- 皮膚の黒ずみ。
三酸化ヒ素曝露の生命を脅かす症状は、体重増加、発熱、呼吸困難、息切れ、胸痛、咳です。
三酸化ヒ素は非常に有毒です人の死にさえつながる可能性のある物質。しかし、それは医療分野でその有用性を持っています。常に予防策を講じる必要があります。

化学反応
三酸化ヒ素は両性です高ヒ素酸化物、およびその水溶液は弱酸性です。したがって、アルカリ性溶液に容易に溶解してヒ酸塩を生成します。塩酸を除いて、酸に溶けにくい。
オゾン、過酸化水素、硝酸などの強力な酸化剤でのみ、+ 5酸性度の五酸化ヒ素Asが形成されます2ああ5..。酸化安定性の点では、三酸化ヒ素は五酸化リンに容易に燃焼する三酸化リンとは異なります。還元により、元素のヒ素またはアルシン(AsH3)

五酸化ヒ素
五酸化物の化学式はAsです2ああ5..。そのモル質量は229.8402g / molです。密度4.32g / cmの白色吸湿性粉末です3..。融点は315°Cに達します。それは分解し始めます。この物質は水とアルコールによく溶けます。酸化ヒ素の特性により、毒性が高く、環境に有害です。それは、より豊富ではなく、毒性が高い無機化合物であり、したがって、より高次の酸化ヒ素(式As2ああ3)
ヒ素は主に毒として知られており、発がん物質。その三酸化物は、無色、無味、無臭の溶液を生成する水溶性粉末です。これは中世の殺人の人気のある方法でした。その使用は今日も続いていますが、平和目的で少量です。



