संतृप्त हाइड्रोकार्बन के समावयवों की रचना करने के तरीके का विश्लेषण करने से पहले, आइए हम कार्बनिक पदार्थों के इस वर्ग की विशेषताओं की पहचान करें।
संतृप्त हाइड्रोकार्बन
कार्बनिक रसायन विज्ञान में, कई वर्ग प्रतिष्ठित हैंसीएक्सएचई। प्रत्येक का अपना सामान्य सूत्र, समजातीय श्रृंखला, गुणात्मक प्रतिक्रियाएँ और अनुप्रयोग होते हैं। अल्केन वर्ग के संतृप्त हाइड्रोकार्बन एकल (सिग्मा) बांडों की विशेषता है। कार्बनिक पदार्थों के इस वर्ग का सामान्य सूत्र CnH2n + 2 है। यह मुख्य रासायनिक गुणों की व्याख्या करता है: प्रतिस्थापन, दहन, ऑक्सीकरण। लगाव पैराफिन की विशेषता नहीं है, क्योंकि इन हाइड्रोकार्बन के अणुओं में बंधन एकल होते हैं।

संवयविता
इस तरह की एक घटना के रूप में समावयवता बताते हैंकार्बनिक पदार्थों की विविधता। समावयवता द्वारा, उस परिघटना को समझने की प्रथा है जिसमें कई कार्बनिक यौगिक होते हैं जिनकी मात्रात्मक संरचना समान होती है (एक अणु में परमाणुओं की संख्या), लेकिन अणु में उनकी अलग व्यवस्था। परिणामी पदार्थों को आइसोमर कहा जाता है। वे हाइड्रोकार्बन के कई वर्गों के प्रतिनिधि हो सकते हैं, और इसलिए रासायनिक गुणों में भिन्न होते हैं। सी परमाणुओं के अल्केन अणु में एक अलग यौगिक संरचनात्मक समरूपता की उपस्थिति की ओर जाता है। एल्केन आइसोमर्स कैसे बनाते हैं? एक निश्चित एल्गोरिथम है जिसके अनुसार किसी दिए गए वर्ग के कार्बनिक पदार्थों के संरचनात्मक आइसोमर्स को चित्रित करना संभव है। एक समान संभावना केवल चार कार्बन परमाणुओं से प्रकट होती है, अर्थात C4H10 ब्यूटेन अणु से।
समरूपता की किस्में
यह समझने के लिए कि फ़ार्मुलों को कैसे लिखना हैआइसोमर्स, इसके प्रकारों का अंदाजा होना जरूरी है। यदि अणु के अंदर समान संख्या में समान परमाणु हैं, एक अलग क्रम में अंतरिक्ष में स्थित हैं, तो हम स्थानिक समरूपता के बारे में बात कर रहे हैं। अन्यथा, इसे स्टीरियोइसोमेरिज्म कहा जाता है। ऐसी स्थिति में केवल संरचनात्मक सूत्रों का उपयोग पर्याप्त नहीं होगा, विशेष प्रक्षेपण या स्थानिक सूत्रों के उपयोग की आवश्यकता होगी। H3C - CH3 (ईथेन) से शुरू होने वाले संतृप्त हाइड्रोकार्बन में अलग-अलग स्थानिक विन्यास होते हैं। यह अणु के अंदर C-C आबंध के साथ घूमने के कारण होता है। यह एक साधारण -बंध है जो गठनात्मक (घूर्णी) समरूपता बनाता है।

पैराफिन का संरचनात्मक समरूपता
आइए बात करते हैं कि अल्केन आइसोमर्स कैसे बनाते हैं।वर्ग में संरचनात्मक समरूपता है, अर्थात कार्बन परमाणु विभिन्न श्रृंखलाएँ बनाता है। अन्यथा, कार्बन परमाणुओं की श्रृंखला में स्थिति बदलने की संभावना को कार्बन कंकाल का समावयवता कहा जाता है।

हेप्टेन के आइसोमर्स
तो, किसी पदार्थ के लिए आइसोमर्स कैसे छोड़ें,रचना C7H16 है? आरंभ करने के लिए, आप सभी कार्बन परमाणुओं को एक लंबी श्रृंखला में व्यवस्थित कर सकते हैं, प्रत्येक के लिए एक निश्चित संख्या में C परमाणु जोड़ सकते हैं। कितने? यह देखते हुए कि कार्बन की संयोजकता चार है, सबसे बाहरी परमाणुओं में तीन हाइड्रोजन परमाणु होंगे, और आंतरिक में दो होंगे। परिणामी अणु में एक रैखिक संरचना होती है, ऐसे हाइड्रोकार्बन को n - हेप्टेन कहा जाता है। अक्षर "n" किसी दिए गए हाइड्रोकार्बन में एक सीधे कार्बन कंकाल को दर्शाता है।
अब हम कार्बन परमाणुओं की व्यवस्था बदलते हैं,C7H16 में सीधी कार्बन श्रृंखला को "छोटा" करते हुए। आइसोमर्स को विस्तारित या संक्षिप्त संरचनात्मक रूप में बनाया जा सकता है। आइए दूसरे विकल्प पर विचार करें। सबसे पहले, हम एक सी परमाणु को विभिन्न स्थितियों में मिथाइल रेडिकल के रूप में व्यवस्थित करते हैं।
हेप्टेन के इस आइसोमर का निम्नलिखित रासायनिक नाम है: 2-मिथाइलहेक्सेन। अब हम रेडिकल को अगले कार्बन परमाणु में "स्थानांतरित" करते हैं। परिणामी संतृप्त हाइड्रोकार्बन को 3-मिथाइलहेक्सेन कहा जाता है।
अगर हम कट्टरपंथी को आगे बढ़ाते हैं,नंबरिंग दाईं ओर से शुरू होगी (हाइड्रोकार्बन रेडिकल शुरुआत के करीब स्थित है), यानी हमें वह आइसोमर मिलेगा जो हमारे पास पहले से है। इसलिए, प्रारंभिक पदार्थ के लिए आइसोमर फ़ार्मुलों की रचना कैसे करें, इस बारे में सोचकर, हम कंकाल को "छोटा" बनाने का प्रयास करेंगे।
शेष दो कार्बन को दो मुक्त कणों - मिथाइल के रूप में दर्शाया जा सकता है।
आइए पहले उन्हें मुख्य श्रृंखला में शामिल विभिन्न कार्बन पर व्यवस्थित करें। आइए हम प्राप्त आइसोमर -२,३ डाइमिथाइलपेंटेन को कॉल करें।
अब एक रेडिकल को उसी स्थान पर छोड़ दें, और दूसरे को मुख्य श्रृंखला के अगले कार्बन परमाणु में स्थानांतरित करें। इस पदार्थ को 2,4 डाइमिथाइलपेंटेन कहा जाता है।
आइए अब एक कार्बन परमाणु पर हाइड्रोकार्बन रेडिकल्स की व्यवस्था करें। पहले, दूसरे के लिए, हमें 2,2 डाइमिथाइलपेंटेन मिलता है। फिर तीसरे स्थान पर, 3.3 डाइमिथाइलपेंटेन प्राप्त किया।
अब हम मुख्य श्रृंखला में चार परमाणु छोड़ते हैं।कार्बन, शेष तीन का उपयोग मिथाइल रेडिकल के रूप में किया जाता है। हम उन्हें इस प्रकार व्यवस्थित करते हैं: दो दूसरे सी परमाणु पर, एक तीसरे कार्बन पर। हम परिणामी आइसोमर कहते हैं: 2,2, 3 ट्राइमेथिलब्यूटेन।
एक उदाहरण के रूप में हेप्टेन का उपयोग करते हुए, हमने चर्चा की है कि संतृप्त हाइड्रोकार्बन के लिए आइसोमरों को सही ढंग से कैसे बनाया जाए। फोटो इसके क्लोरीन डेरिवेटिव के ब्यूटेन 6 के लिए संरचनात्मक आइसोमर्स के उदाहरण दिखाता है।

अल्केनेस
कार्बनिक पदार्थों के इस वर्ग में एक आम हैसूत्र CnH2n। संतृप्त सीसी बांड के अलावा, इस वर्ग में एक दोहरा बंधन भी होता है। वह वह है जो इस श्रृंखला के मुख्य गुणों को निर्धारित करती है। आइए बात करते हैं कि एल्केन्स के आइसोमर्स को कैसे छोड़ा जाए। आइए संतृप्त हाइड्रोकार्बन से उनके अंतरों को पहचानने का प्रयास करें। मुख्य श्रृंखला (संरचनात्मक सूत्रों) के आइसोमेरिज्म के अलावा, कार्बनिक हाइड्रोकार्बन के इस वर्ग के प्रतिनिधियों को तीन और प्रकार के आइसोमर्स की भी विशेषता है: ज्यामितीय (सीआईएस और ट्रांसफॉर्म), कई बॉन्ड पोजीशन, और इंटरक्लास आइसोमेरिज्म (साइक्लोअल्केन्स के साथ)।

आइसोमर्स C6H12
आइए यह पता लगाने की कोशिश करें कि c6h12 आइसोमर्स की रचना कैसे की जाती है, इस तथ्य को ध्यान में रखते हुए कि इस सूत्र वाला पदार्थ एक ही बार में दो वर्गों के कार्बनिक पदार्थों से संबंधित हो सकता है: एल्केन्स, साइक्लोअल्केन्स।
सबसे पहले, आइए सोचें कि आइसोमर्स कैसे बनाएंयदि अणु में दोहरा बंधन है तो एल्केन्स। हम एक सीधी कार्बन श्रृंखला डालते हैं, पहले कार्बन परमाणु के बाद कई बंधन लगाते हैं। आइए न केवल 6Н12 के समावयवों की रचना करने का प्रयास करें, बल्कि पदार्थों के नाम भी लिखें। यह पदार्थ हैक्सिन-1 है। संख्या द्विआबंध के अणु में स्थिति दर्शाती है। जब यह कार्बन श्रृंखला के साथ आगे बढ़ता है, तो हमें हेक्सिन -2, साथ ही हेक्सिन - 3 . मिलता है
अब आइए विचार करें कि मुख्य श्रृंखला में परमाणुओं की संख्या को बदलते हुए, इस सूत्र के लिए आइसोमर्स की रचना कैसे करें।
सबसे पहले, कार्बन कंकाल को एक से छोटा करते हैंकार्बन परमाणु, इसे मिथाइल रेडिकल माना जाएगा। हम पहले सी परमाणु के बाद दोहरे बंधन को छोड़ देंगे। व्यवस्थित नामकरण के अनुसार, परिणामी आइसोमर का निम्नलिखित नाम होगा: 2 मिथाइलपेंटीन - 1. अब हम दोहरे बंधन की स्थिति को छोड़कर, मुख्य श्रृंखला के साथ हाइड्रोकार्बन मूलक को स्थानांतरित करते हैं। अपरिवर्तित। इस शाखित असंतृप्त हाइड्रोकार्बन को 3 मेथिलपेन्टीन -1 कहा जाता है।
मुख्य श्रृंखला और दोहरे बंधन की स्थिति को बदले बिना एक और आइसोमर संभव है: 4 मिथाइलपेंटीन -1।
रचना C6H12 के लिए, आप स्थानांतरित करने का प्रयास कर सकते हैंमुख्य श्रृंखला को बदले बिना, पहली से दूसरी स्थिति में दोहरा बंधन इस मामले में, रेडिकल दूसरे सी परमाणु से शुरू होने वाले कार्बन कंकाल के साथ आगे बढ़ेगा। इस आइसोमर को 2 मेथिलपेन्टिन -2 कहा जाता है। इसके अलावा, आप तीसरे कार्बन परमाणु के CH3 रेडिकल को 3 मिथाइलपेंटीन-2 . प्राप्त करने के लिए रख सकते हैं
यदि हम इस श्रृंखला में एक परमाणु के चौथे कार्बन पर एक रेडिकल रखते हैं, तो एक पापी कार्बन कंकाल के साथ एक और नया असंतृप्त हाइड्रोकार्बन पदार्थ बनता है - 4 मिथाइलपेंटीन -2।
मुख्य श्रृंखला में सी की संख्या में और कमी के साथ, आप एक और आइसोमर प्राप्त कर सकते हैं।
हम पहले कार्बन परमाणु के बाद दोहरा बंधन छोड़ते हैं, और मुख्य श्रृंखला के तीसरे सी परमाणु में दो रेडिकल डालते हैं, हमें 3.3 डाइमिथाइलुटीन -1 मिलता है।
आइए अब रेडिकल्स को आसन्न कार्बन पर डालते हैंपरमाणु, दोहरे बंधन की स्थिति को बदले बिना, हमें 2,3 डाइमिथाइलब्यूटीन -1 मिलता है। आइए, मुख्य श्रृंखला के आकार को बदले बिना, दोहरे बंधन को दूसरी स्थिति में ले जाने का प्रयास करें। इस मामले में, हम केवल २ और ३ सी परमाणुओं पर रेडिकल की आपूर्ति कर सकते हैं, २,३ डाइमिथाइलब्यूटिन -2 प्राप्त कर सकते हैं।
इस एल्केन के लिए कोई अन्य संरचनात्मक आइसोमर्स नहीं हैं, उनके आविष्कार के किसी भी प्रयास से एएम बटलरोव के कार्बनिक पदार्थों की संरचना के सिद्धांत का उल्लंघन होगा।

C6H12 . के स्थानिक समावयवी
अब आइए जानें कि स्थानिक समावयवता के संदर्भ में समावयवी और समजातीय रचना कैसे करें। यह समझना महत्वपूर्ण है कि सीआईएस और एल्केन्स परिवर्तन केवल दोहरे बंधन 2 और 3 की स्थिति के लिए ही संभव हैं।
जब हाइड्रोकार्बन रेडिकल एक ही तल में होते हैं, तो सीआईएस बनता है - हेक्सिन -2 को मापना, और जब रेडिकल अलग-अलग विमानों में स्थित होते हैं, तो हेक्सिन का ट्रांस-फॉर्म 2 होता है।
इंटरक्लास आइसोमर्स C6H12
आइसोमर्स बनाने के तरीके पर चर्चा करना औरसमरूपता, हमें इस तरह के एक प्रकार के बारे में नहीं भूलना चाहिए जैसे कि इंटरक्लास आइसोमेरिज्म। एथिलीन श्रेणी के असंतृप्त हाइड्रोकार्बनों के लिए जिनका सामान्य सूत्र CnH2n होता है, ऐसे समावयवी साइक्लोऐल्केन होते हैं। हाइड्रोकार्बन के इस वर्ग की एक विशेषता कार्बन परमाणुओं के बीच संतृप्त एकल बंधों के साथ एक चक्रीय (बंद) संरचना की उपस्थिति है। साइक्लोहेक्सेन, मिथाइलसाइक्लोपेंटेन, डाइमिथाइलसाइक्लोब्यूटेन, ट्राइमेथिलसाइक्लोप्रोपेन के लिए सूत्र तैयार किए जा सकते हैं।
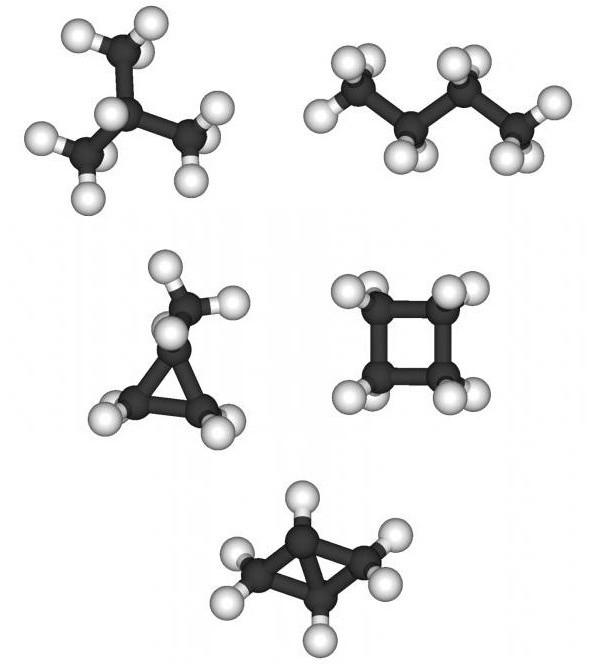
निष्कर्ष
कार्बनिक रसायन बहुआयामी और रहस्यमय है।कार्बनिक पदार्थों की मात्रा अकार्बनिक यौगिकों की संख्या से सैकड़ों गुना अधिक है। इस तथ्य को आइसोमेरिज्म जैसी अनूठी घटना के अस्तित्व से आसानी से समझाया जा सकता है। यदि समान समजातीय श्रेणी में गुण और संरचना में समान पदार्थ हों, तो जब श्रृंखला में कार्बन परमाणुओं की स्थिति बदलती है, तो नए यौगिक दिखाई देते हैं, जिन्हें आइसोमर्स कहा जाता है। कार्बनिक पदार्थों की रासायनिक संरचना के सिद्धांत की उपस्थिति के बाद ही सभी हाइड्रोकार्बन को वर्गीकृत करना, प्रत्येक वर्ग की बारीकियों को समझना संभव था। इस सिद्धांत के प्रावधानों में से एक सीधे समरूपता की घटना से संबंधित है। महान रूसी रसायनज्ञ यह समझने, समझाने, साबित करने में सक्षम थे कि किसी पदार्थ के रासायनिक गुण, उसकी प्रतिक्रिया गतिविधि और व्यावहारिक अनुप्रयोग कार्बन परमाणुओं की व्यवस्था पर निर्भर करते हैं। यदि हम संतृप्त एल्केन्स और असंतृप्त एल्केन्स द्वारा गठित आइसोमर्स की संख्या की तुलना करते हैं, तो निस्संदेह अल्केन्स लीड में हैं। यह इस तथ्य से समझाया गया है कि उनके अणुओं में एक दोहरा बंधन होता है। यह वह है जो कार्बनिक पदार्थों के इस वर्ग को न केवल विभिन्न प्रकार और संरचनाओं के अल्केन्स बनाने की अनुमति देता है, बल्कि साइक्लोअल्केन्स के साथ मेक्लास आइसोमेरिज्म के बारे में भी बात करता है।





