Úvod
Podíváme se zblízka na dusíkPeriodická tabulka chemických prvků DI Mendeleeva, je vidět, že má variabilní valenci. To znamená, že dusík tvoří s kyslíkem několik binárních sloučenin najednou. Některé z nich byly objeveny nedávno a některé byly studovány nahoru a dolů. Existují nestabilní a stabilní oxidy dusíku. Chemické vlastnosti každé z těchto látek jsou zcela odlišné, proto při jejich studiu je třeba vzít v úvahu nejméně pět oxidů dusíku. To bude diskutováno v dnešním článku.
Oxid dusnatý (I)

Vlastnosti
Za normálních podmínek je to bezbarvý plyn,s nasládlou vůní. Může být rozpuštěn vodou, ethanolem, etherem a kyselinou sírovou. Pokud se plynný monovalentní oxid dusnatý zahřeje na teplotu místnosti pod tlakem 40 atmosfér, zahustí se na bezbarvou kapalinu. Je to oxid nevytvářející sůl, který se během zahřívání rozkládá a projevuje se v reakcích jako redukční činidlo.
Příjem
Tento oxid se vytvoří, když se zahřeje suchý dusičnan amonný. Dalším způsobem, jak toho dosáhnout, je termickým rozkladem směsi sulfamidu a kyseliny dusičné.
přihláška
Používá se jako lék nainhalační anestézie, potravinářský průmysl zná tento oxid jako přísadu E942. Zlepšuje také technické vlastnosti spalovacích motorů.
Oxid dusnatý (II)

Vlastnosti
Za normálních podmínek vypadá jako bezbarvýplyn, který je špatně rozpustný ve vodě. Je těžké jej zkapalnit, ale v pevném a kapalném stavu je modrý. Tento oxid může být oxidován atmosférickým kyslíkem
Příjem
Je to docela snadné si to, pro to musíte zahřát až 1200-1300oSe směsí dusíku a kyslíku. V laboratorních podmínkách se tvoří najednou v několika experimentech:
- Reakce mědi a 30% roztoku kyseliny dusičné.
- Reakce mezi chloridem železitým, dusitanem sodným a kyselinou chlorovodíkovou.
- Reakce dusitých a jodovodíkových kyselin.
přihláška
Jedná se o jednu z látek, ze které se získává kyselina dusičná.
Oxid dusnatý (III)

Vlastnosti
Za normálních podmínek je to kapalina, která má modrou barvu a za standardních podmínek je to bezbarvý plyn. Čistý oxid existuje pouze v pevném stavu agregace.
Příjem
Vzniká interakcí 50% kyseliny dusičné a pevného oxidu trojmocného arsenu (může být také nahrazen škrobem).
přihláška
Pomocí této látky se v laboratořích získává kyselina dusitá a její soli.
Oxid dusnatý (IV)
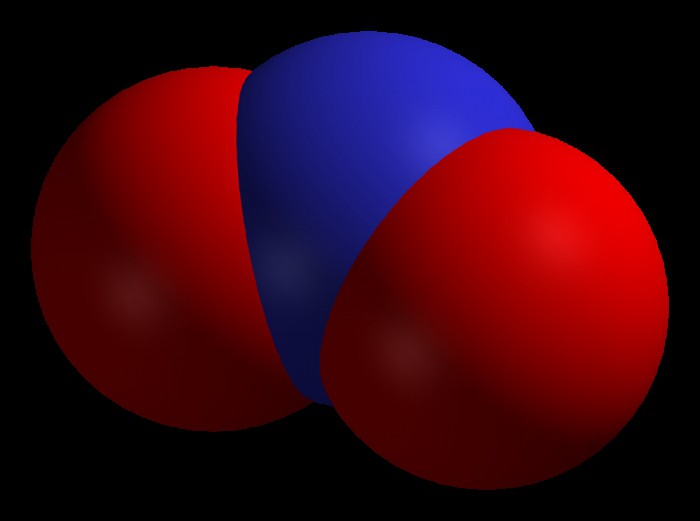
Vlastnosti
Příjmení odpovídá jedné z jeho vlastností. Koneckonců, tento oxid má formu buď červenohnědého plynu nebo nažloutlé kapaliny. Vyznačuje se vysokou chemickou aktivitou.
Příjem
Tento oxid se získává interakcí kyseliny dusičné a mědi, jakož i při tepelném rozkladu dusičnanu olovnatého.
přihláška
S jeho pomocí se vyrábí kyselina sírová a dusičná, kapalné raketové palivo a směsné výbušniny se oxidují.
Oxid dusnatý (V)

Vlastnosti
Má vzhled bezbarvých a vysoce těkavých krystalů. Mohou se roztavit při 32,3oC.
Příjem
Tento oxid je tvořen několika reakcemi:
- Dehydratace kyseliny dusičné pentavalentním oxidem fosforečným.
- Přechod suchého chloru na dusičnan stříbrný.
- Interakce ozonu s čtyřmocným oxidem dusíku.
přihláška
Vzhledem ke své extrémní nestabilitě se nepoužívá nikde v čisté formě.
Závěr
V chemii je devět oxidů dusíku,výše uvedené jsou pouze klasické sloučeniny tohoto prvku. Další čtyři jsou, jak již bylo zmíněno, nestabilní látky. Všechny však spojuje jedna vlastnost - vysoká toxicita. Emise oxidů dusíku do ovzduší vedou ke zhoršení zdraví lidí žijících v blízkosti průmyslových chemických závodů. Příznaky otravy kteroukoli z těchto látek jsou toxický plicní edém, narušení centrálního nervového systému a poškození krve, jehož příčinou je vazba hemoglobinu. S oxidy dusíku proto musí být zacházeno opatrně a ve většině případů musí být použity ochranné prostředky.





