Fiziksel dünyanın olayları ayrılmaz bir şekilde birbiriyle bağlantılıdır.sıcaklıktaki değişiklikler. Her insan onu erken çocukluk döneminde, buzun soğuk olduğunu ve kaynayan suyun yaktığını anladığında tanır. Aynı zamanda, sıcaklık değişim süreçlerinin anında gerçekleşmediği anlayışı gelir. Daha sonra okulda öğrenci, ısı hareketi ile ilgili olanı öğrenir. Ve sıcaklıkla ilgili süreçler, fiziğin bütün bir bölümü tahsis edilir.

sıcaklık nedir?
Bu bilimsel kavram, sıradan olanın yerini almak üzere tanıtıldı.terimler. Sıcak, soğuk veya ılık gibi kelimeler günlük yaşamda sürekli olarak karşımıza çıkar. Hepsi vücut ısısının derecesinden bahsediyor. Fizikte bu şekilde tanımlanır, ancak skaler bir miktar olduğu eklenerek. Sonuçta, sıcaklığın yönü yoktur, sadece sayısal bir değeri vardır.
Uluslararası birim sisteminde (SI), sıcaklıkSantigrat derece (ºС) cinsinden ölçülür. Ancak termal olayları tanımlayan birçok formülde onu Kelvin (K)'ye çevirmek gerekir. Bunun için basit bir formül var: T = t + 273. İçinde T, Kelvin cinsinden sıcaklık ve t, Santigrat cinsindendir. Kelvin ölçeği, mutlak sıfır sıcaklık kavramıyla ilişkilidir.
Birkaç sıcaklık ölçeği daha var.Avrupa ve Amerika'da örneğin Fahrenheit (F) kullanılır. Bu nedenle, onları Celsius cinsinden yazabilmelidirler. Bunu yapmak için, F'deki okumalardan 32'yi çıkarmak ve ardından 1.8'e bölmek gerekir.

Ev deneyi
Açıklamasında sıcaklık, termal hareket gibi kavramların bilinmesi gerekmektedir. Ve bu deneyi yapmak kolaydır.
Onun için üç kap almanız gerekiyor.Ellerinize kolayca sığacak kadar büyük olmalıdırlar. Onları farklı sıcaklıklarda su ile doldurun. İlk olarak, çok soğuk olmalıdır. İkincisinde - ısındı. Bir eli tutmanın mümkün olacağı üçüncüsüne sıcak su dökün.
Şimdi deneyimin kendisi. Sol elinizi bir soğuk su kabına ve sağ elinizi en sıcak olana batırın. Birkaç dakika bekleyin. Onları çıkarın ve hemen bir ılık su kabına batırın.
Sonuç beklenmedik olacaktır.Sol el suyun sıcak olduğunu, sağ el ise soğuk su hissini hissedecektir. Bunun nedeni, başlangıçta ellerin içine daldırıldığı sıvılarla termal dengenin kurulmasıdır. Ve sonra bu denge büyük ölçüde bozulur.
Moleküler kinetik teorinin temel prensipleri
Tüm termal olayları açıklar. Ve bu ifadeler oldukça basittir. Bu nedenle termal hareketten bahsederken bu hükümlerin bilinmesi gerekir.
Öncelikle:maddeler, birbirinden belirli bir uzaklıkta bulunan en küçük parçacıklardan oluşur. Ayrıca, bu parçacıklar hem moleküller hem de atomlar olabilir. Ve aralarındaki mesafe, parçacık boyutundan birçok kat daha fazladır.
İkincisi: tüm maddelerde moleküllerin asla durmayan bir termal hareketi vardır. Bu durumda, parçacıklar rastgele (kaotik) hareket eder.
Üçüncüsü: parçacıklar birbirleriyle etkileşime girer. Bu eylem, çekim ve itme kuvvetlerinden kaynaklanmaktadır. Değerleri, parçacıklar arasındaki mesafeye bağlıdır.
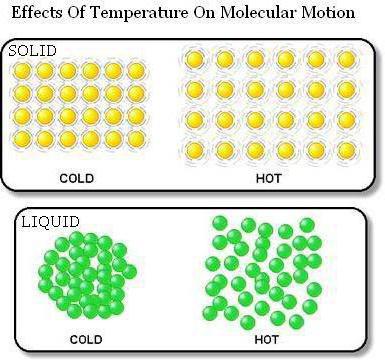
ICB'nin ilk hükmünün teyidi
cisimlerin taneciklerden oluştuğunun kanıtıaralarında boşluklar bulunan, termal genleşmeleri hizmet eder. Böylece, vücut ısıtıldığında boyutu artar. Bu, parçacıkların birbirinden uzaklaştırılması nedeniyle olur.
Yukarıdakilerin bir başka teyididifüzyon. Yani, bir maddenin moleküllerinin diğerinin parçacıkları arasına nüfuz etmesi. Üstelik bu hareketin karşılıklı olduğu ortaya çıkıyor. Difüzyon, moleküller birbirinden ne kadar hızlı olursa o kadar hızlı gerçekleşir. Bu nedenle gazlarda karşılıklı penetrasyon sıvılardan çok daha hızlı gerçekleşir. Ve katılarda difüzyon yıllar alır.
Bu arada, ikinci süreç aynı zamanda termal hareketi de açıklar. Sonuçta, maddelerin birbirine karşılıklı nüfuzu, dışarıdan herhangi bir müdahale olmadan gerçekleşir. Ancak vücudu ısıtarak hızlandırılabilir.
ICB'nin ikinci hükmünün teyidi
var olduğunun açık bir kanıtıtermal hareket, parçacıkların Brown hareketidir. Asılı parçacıklar için, yani maddenin moleküllerinden önemli ölçüde daha büyük olanlar için kabul edilir. Bu parçacıklar toz lekeleri veya tanecikler olabilir. Ve suya veya gaza yerleştirilmeleri gerekiyor.
Ağırlıklı düzensiz hareketin nedenimoleküllerin her yönden etki ettiği gerçeğindeki parçacıklar. Eylemleri düzensizdir. Etkilerin büyüklüğü zamanın her anında farklıdır. Bu nedenle, ortaya çıkan kuvvet şu veya bu yöne yönlendirilir.
Moleküllerin termal hareket hızı hakkında konuşursak, bunun için özel bir isim vardır - ortalama kare kök. Aşağıdaki formül kullanılarak hesaplanabilir:
v = √ [(3kT) / m0].
İçinde T, Kelvin cinsinden sıcaklık, m0 Bir molekülün kütlesi, k Boltzmann sabitidir (k = 1.38 * 10-23 J / K).

ICB'nin üçüncü hükmünün teyidi
Parçacıklar çeker ve iter. Termal hareketle ilgili birçok işlemi açıklamada bu bilginin önemli olduğu ortaya çıkıyor.
Sonuçta, etkileşim kuvvetleri agregaya bağlıdır.Maddenin durumu. Bu nedenle, gazlar pratik olarak bunlara sahip değildir, çünkü parçacıklar o kadar çok uzaklaştırılır ki etkileri ortaya çıkmaz. Sıvılarda ve katılarda algılanabilirler ve maddenin hacminin korunmasını sağlarlar. İkincisinde, formda kalmayı da garanti ederler.
Çekim kuvvetlerinin varlığının kanıtı veitme, cisimlerin deformasyonu sırasında elastik kuvvetlerin ortaya çıkmasıdır. Böylece, uzama ile moleküller arasındaki çekim kuvvetleri ve sıkıştırma ile itme artar. Ancak her iki durumda da vücudu orijinal şekline döndürürler.

Termal hareketin ortalama enerjisi
MKT'nin temel denkleminden yazılabilir:
(pV) / N = (2E) / 3.
Bu formülde p basınç, V hacim, N molekül sayısı ve E ortalama kinetik enerjidir.
Öte yandan, bu denklem şu şekilde yazılabilir:
(pV) / N = kT.
Bunları birleştirirseniz, aşağıdaki eşitliği elde edersiniz:
(2E) / 3 = kT.
Bundan, moleküllerin ortalama kinetik enerjisi için aşağıdaki formül çıkar:
E = (3kT) / 2.
Buradan enerjinin orantılı olduğu görülebilir.maddenin sıcaklığı. Yani, ikincisi yükseldiğinde, parçacıklar daha hızlı hareket eder. Mutlak sıfırdan farklı bir sıcaklık olduğu sürece var olan termal hareketin özü budur.








