Händelserna i den fysiska världen är oupplösligt förbundna medtemperaturförändringar. Varje person blir bekant med det i tidig barndom, när de förstår att is är kall och kokande vatten brinner. Samtidigt blir det tydligt att temperaturförändringsprocesser inte inträffar omedelbart. Senare, i skolan, får eleven veta att detta är kopplat till termisk rörelse. Och en hel del av fysiken är tillägnad processer relaterade till temperatur.

Vad är temperatur?
Detta vetenskapliga koncept introducerades för att ersätta vanligavillkor. I vardagen dyker det ständigt upp ord som varmt, kallt eller varmt. De talar alla om graden av uppvärmning av kroppen. Det är precis så det definieras i fysiken, bara med tillägget att det är en skalär storhet. Temperaturen har trots allt ingen riktning, utan bara ett numeriskt värde.
I det internationella enhetssystemet (SI), temperaturmätt i grader Celsius (ºC). Men i många formler som beskriver termiska fenomen krävs det att det konverteras till Kelvin (K). Det finns en enkel formel för detta: T = t + 273. I den är T temperaturen i Kelvin och t är i Celsius. Förknippat med Kelvin-skalan är begreppet absolut nolltemperatur.
Det finns flera andra temperaturskalor.I Europa och Amerika, till exempel, används Fahrenheit (F). Därför måste de kunna skrivas i Celsius. För att göra detta, subtrahera 32 från avläsningarna i F och dividera det sedan med 1,8.

Hemexperiment
Dess förklaring kräver kunskap om begrepp som temperatur och termisk rörelse. Och detta experiment är lätt att utföra.
Det kommer att krävas tre behållare.De ska vara tillräckligt stora för att lätt passa dina händer. Fyll dem med vatten med olika temperaturer. I den första ska det vara väldigt kallt. I den andra - uppvärmd. Häll varmt vatten i den tredje, så att du kan hålla handen i den.
Nu själva upplevelsen. Placera vänster hand i en behållare med kallt vatten, höger hand i den hetaste. Vänta ett par minuter. Ta ut dem och doppa dem omedelbart i en behållare med varmt vatten.
Resultatet kommer att bli oväntat.Vänster hand kommer att kännas som om vattnet är varmt, höger hand kommer att kännas som att vattnet är kallt. Detta beror på det faktum att termisk jämvikt först etableras med de vätskor som händerna initialt är nedsänkta i. Och så störs den här balansen plötsligt.
Grundläggande principer för molekylär kinetisk teori
Den beskriver alla termiska fenomen. Och dessa uttalanden är ganska enkla. Därför, när man talar om termisk rörelse, är det nödvändigt att känna till dessa bestämmelser.
Först:ämnen bildas av små partiklar som ligger på något avstånd från varandra. Dessutom kan dessa partiklar vara både molekyler och atomer. Och avståndet mellan dem är många gånger större än partikelstorleken.
För det andra: i alla ämnen finns det termisk rörelse av molekyler, som aldrig slutar. Partiklarna rör sig slumpmässigt (kaotiskt).
För det tredje: partiklar interagerar med varandra. Denna handling beror på krafterna av attraktion och avstötning. Deras storlek beror på avståndet mellan partiklarna.
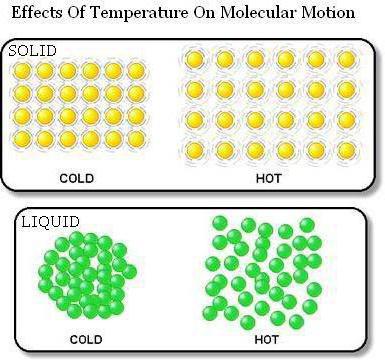
Bekräftelse av den första bestämmelsen i IKT
Bevis på att kroppar är gjorda av partiklar,mellan vilka det finns luckor, tjänar deras termiska expansion. Så när en kropp värms upp ökar dess storlek. Detta sker på grund av att partiklarna rör sig bort från varandra.
En annan bekräftelse på detta ärdiffusion. Det vill säga penetrering av molekyler av ett ämne mellan partiklar av ett annat. Dessutom visar sig denna rörelse vara ömsesidig. Diffusionen fortskrider snabbare ju längre molekylerna befinner sig från varandra. Därför kommer ömsesidig penetration att ske mycket snabbare i gaser än i vätskor. Men i fasta ämnen tar diffusion år.
Förresten, den senare processen förklarar också termisk rörelse. När allt kommer omkring sker den ömsesidiga penetrationen av ämnen i varandra utan ingripande utifrån. Men det kan påskyndas genom att värma upp kroppen.
Bekräftelse av den andra bestämmelsen i IKT
Tydliga bevis på att det finnstermisk rörelse är Brownsk rörelse av partiklar. Det övervägs för suspenderade partiklar, det vill säga för de som är betydligt större än ämnets molekyler. Dessa partiklar kan vara dammpartiklar eller korn. Och de ska placeras i vatten eller gas.
Anledningen till den oberäkneliga rörelsen av den viktadepartiklar är att molekyler verkar på den från alla håll. Deras agerande är slumpmässigt. Storleken på effekterna är olika vid varje tidpunkt. Därför riktas den resulterande kraften i den ena eller andra riktningen.
Om vi pratar om hastigheten för termisk rörelse av molekyler, så finns det ett speciellt namn för det - rotmedelkvadrat. Det kan beräknas med formeln:
v = √[(3kT)/m0].
I den är T temperaturen i Kelvin, m0 - massa av en molekyl, k - Boltzmann konstant (k=1,38*10-23 J/K).

Bekräftelse av den tredje bestämmelsen i IKT
Partiklar attraherar och stöter bort. För att förklara många processer förknippade med termisk rörelse visar sig denna kunskap vara viktig.
När allt kommer omkring beror växelverkanskrafterna på aggregatetmateriens tillstånd. Således har gaser praktiskt taget inte dem, eftersom partiklarna avlägsnas så mycket att deras effekt inte visar sig. I vätskor och fasta ämnen är de märkbara och säkerställer bevarandet av ämnets volym. I det senare garanterar de också bibehållen form.
Bevis på att det finns attraktiva krafter ochrepulsion är uppkomsten av elastiska krafter under deformation av kroppar. Således, med förlängning, ökar attraktionskrafterna mellan molekyler, och med kompression ökar frånstötningskrafterna. Men i båda fallen återställer de kroppen till sin ursprungliga form.

Genomsnittlig energi för termisk rörelse
Det kan skrivas från den grundläggande MKT-ekvationen:
(pV)/N = (2E)/3.
I denna formel är p tryck, V är volym, N är antalet molekyler, E är genomsnittlig kinetisk energi.
Å andra sidan kan denna ekvation skrivas så här:
(pV)/N = kT.
Om vi kombinerar dem får vi följande likhet:
(2E)/3 = kT.
Av den följer följande formel för den genomsnittliga kinetiska energin hos molekyler:
E = (3kT)/2.
Detta visar att energin är proportionellämnets temperatur. Det vill säga när den senare ökar rör sig partiklarna snabbare. Detta är kärnan i termisk rörelse, som existerar så länge det finns en temperatur som skiljer sig från absoluta nollpunkten.








