תרכובות בינאריות הן חומרים הנוצרים על ידי שני יסודות כימיים שונים. מונח זה משמש לציון ההרכב האיכותי והכמותי של תרכובות אנאורגניות.
תרכובות כימיות בינאריות נחשבות חשובותאובייקט בחקר טבעם של חומרים. כאשר מתארים אותם, נעשה שימוש במושגים הבאים: קיטוב קשר, מצב חמצון, ערכיות. מונחים כימיים אלו מאפשרים להבין את מהות היווצרותו של קשר כימי, את התכונות המבניות של חומרים אנאורגניים.
הבה נבחן את המחלקות העיקריות של תרכובות בינאריות, את תכונות המבנה והתכונות הכימיות שלהן, וכמה תחומים של היישום התעשייתי שלהן.

תחמוצות
סוג זה של חומרים אנאורגניים הוא הנפוץ ביותר בטבע. בין הנציגים הידועים של קבוצת תרכובות זו, אנו מדגישים:
- תחמוצת סיליקון (חול נהר);
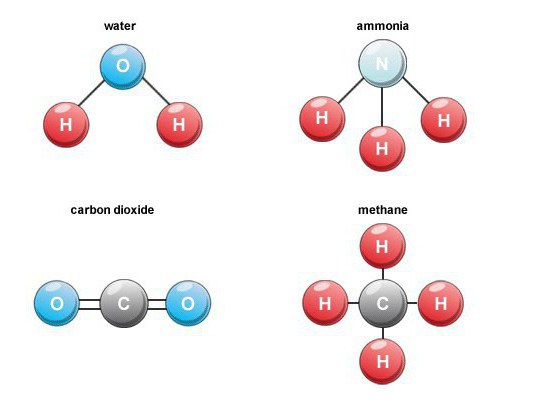
- תחמוצת מימן (מים);
- פחמן דו חמצני;
- חימר (תחמוצת אלומיניום);
- עפרות ברזל (תחמוצות ברזל).
תרכובות בינאריות כאלה הן חומרים מורכבים, המכילים בהכרח חמצן, המציג מצב חמצון של -2.
מצב מצטבר של תחמוצות
תרכובות של נחושת, סידן, ברזל הםמוצקים גבישיים. באותו מצב צבירה יש תחמוצות של כמה לא מתכות, כגון גופרית משושה, זרחן מחומש, סיליקון. הנוזל בתנאים רגילים הוא מים. הרוב המכריע של תרכובות החמצן של לא-מתכות הן גזים.
תכונות חינוך
נוצרות תרכובות חמצן בינאריות רבותבטבע. לדוגמה, במהלך בעירה של דלק, נשימה, ריקבון של חומר אורגני, פחמן דו חמצני (פחמן חד חמצני 4) נוצר. באוויר, תכולת הנפח שלו היא כ-0.03 אחוז.
תרכובות בינאריות דומות הן מוצריםפעילות הרי געש, כמו גם חלק בלתי נפרד ממים מינרליים. פחמן דו חמצני אינו תומך בעירה, ולכן תרכובת כימית זו משמשת לכיבוי שריפות.
תרכובות מימן נדיפות
תרכובות בינאריות כאלה הן קבוצה חשובהחומרים המכילים מימן. בין הנציגים בעלי החשיבות התעשייתית, נציין מתאן, מים, מימן גופרתי, אמוניה והלידי מימן.
כמה תרכובות מימן נדיפות קיימות במי הקרקע ובאורגניזמים חיים, אז אנחנו יכולים לדבר על תפקידם הגיאוכימי והביוכימי.
כדי להרכיב תרכובות בינאריות מסוג זה, מימן בעל ערכיות מונח במקום הראשון. היסוד השני הוא לא מתכת בעלת מצב חמצון שלילי.
כדי לסדר אינדקסים בצירוף בינאריבין ערכיות, הכפולה הנמוכה ביותר נקבעת. מספר האטומים של כל יסוד נקבע על ידי חלוקתו בערכיות של כל יסוד שהוא חלק מהתרכובת.

מימן כלורי
שקול את הנוסחאות של תרכובות בינאריות:מימן כלורי ואמוניה. החומרים הללו הם החשובים לתעשייה הכימית המודרנית. HCl בתנאים רגילים הוא תרכובת גזית, מסיס מאוד במים. לאחר התמוססות גז המימן כלורי נוצרת חומצה הידרוכלורית המשמשת בתהליכים כימיים רבים ושרשראות ייצור.
תרכובת בינארית זו מצויה במיץ הקיבה של בני אדם ובעלי חיים, ומהווה מחסום בפני חיידקים פתוגניים החודרים לקיבה עם מזון.
בין תחומי היישום העיקריים של חומצה הידרוכלורית, אנו מפרטים ייצור כלורידים, סינתזה של מוצרים המכילים כלור, כבישת מתכות, ניקוי צינורות מתחמוצות וקרבונטים ותעשיית העור.
אמוניה בעלת הנוסחה NH3, הוא גז חסר צבע עםריח חריף ספציפי. מסיסותו הבלתי מוגבלת במים מאפשרת להשיג אמוניה, המבוקשת ברפואה. בטבע, תרכובת בינארית זו נוצרת במהלך ריקבון של מוצרים אורגניים, המכילים חנקן.

סיווג תחמוצת
תרכובת בינארית המכילה חמצן של מתכת בעלת ערכיות של 1 או 2 היא התחמוצת הבסיסית. לדוגמה, קבוצה זו כוללת תחמוצות של מתכות אלקליות ואדמה אלקליין.
תחמוצות של לא מתכות, כמו גם מתכות בעלות ערכיות גדולה מ-4, הן תרכובות חומציות.
בהתאם לתכונות הכימיות, נציגי מחלקה זו מחולקים לקבוצות יוצרות מלח ולא יוצרות מלח.
בין הנציגים האופייניים לקבוצה השנייה, נציין פחמן חד חמצני (CO), תחמוצת חנקן 1 (NO).
יצירת שמות שיטתיים של תרכובות
בין המשימות המוצעות לבוגרים שעובריםמבחן המדינה בכימיה, יש גם את זה: "חבר את הנוסחאות המולקולריות של תרכובות חמצן בינאריות אפשריות של גופרית (חנקן, זרחן)". על מנת להתמודד עם המשימה, יש צורך לקבל מושג לא רק על האלגוריתם, אלא גם על התכונות של המינוח של מחלקה זו של חומרים אנאורגניים.
כאשר יוצרים שם של בינאריתרכובות, מציינים בתחילה את היסוד הממוקם בצד ימין בנוסחה, ומוסיפים את הסיומת "id". לאחר מכן, ציין את שם האלמנט הראשון. לתרכובות קוולנטיות מתווספות קידומות שבאמצעותן ניתן לקבוע יחס כמותי בין החלקים המרכיבים תרכובת בינארית.
למשל SO3 - טריאוקסיד גופרית, N2הו4 – דיניטרוגן טטרוקסיד, I2CL6 – דיודה הקסכלוריד.
אם תרכובת בינארית מכילה יסוד כימי המסוגל להציג מצבי חמצון שונים, מצב החמצון מצוין בסוגריים אחרי שם התרכובת.
לדוגמה, שתי תרכובות ברזל שונות בשם: FeCL3 - תחמוצת ברזל (3), FeCL2 - תחמוצת ברזל (2).
עבור הידידים, במיוחד אלמנטים לא מתכתיים, משתמשים בשמות טריוויאליים. כן, ח2O - מים, HCL - מימן כלורי, HI - יודיד מימן, HF - חומצה הידרופלואורית.

קטיונים
יונים חיוביים של אותם אלמנטיםמסוגלים ליצור רק יון יציב אחד, תנו את אותם שמות כמו הסמלים עצמם. אלה כוללים את כל נציגי הקבוצה הראשונה והשנייה של המערכת המחזורית של מנדלייב.
לדוגמה, לקטיונים של נתרן ומגנזיום יש את הצורה: Na+, Mg2+. רכיבי מעבר מסוגלים ליצור מספר סוגים של קטיונים, ולכן השם חייב לציין את הערכיות המופיעה בכל מקרה בודד.
אניונים
עבור אניונים פשוטים (מונטומיים) ומורכבים (פוליאטומיים), משתמשים בסיומת -id.
אוקסוניון נפוץ של מסוייםאלמנט הוא הסיומת -am. עבור אוקסוניון של יסוד שנמצא בנוסחה עם מצב חמצון נמוך יותר, משתמשים בסיומת -it. הקידומת hypo- משמשת למצב החמצון המינימלי, ו-per- משמשת לערך המקסימלי. לדוגמה, יון O2- הוא יון תחמוצת, ו-O- - מי חמצן.
ישנם גם שמות טריוויאליים שונים להידרידים. לדוגמה, נ2X4 שנקרא הידרזין, ו-PH3 שנקרא פוספין.
לאוקסוניונים המכילים גופרית יש את השמות הבאים:
- עם42- - סולפט;
- ג2הו32- - תיוסולפט;
- NCS- - תיאוציאנט.
מלח
מבחנים סופיים רבים בכימיה מציעיםהמשימה הבאה: "צור נוסחאות לתרכובות בינאריות של מתכות." אם תרכובות כאלה מכילות אניונים של כלור, ברום, יוד, תרכובות כאלה נקראות הלידים ושייכות למחלקת המלחים. בעת ניסוח תרכובות בינאריות אלה, המתכת מונחת תחילה, ואחריה את יון ההליד המתאים.
כדי לקבוע את מספר האטומים של כל יסוד, נמצא הכפולה הקטנה ביותר בין הערכיות; כאשר מחלקים מתקבלים מדדים.
לתרכובות אלו נקודת התכה גבוהה.ורותחים, מסיסות טובה במים, בתנאים רגילים הם מוצקים. לדוגמה, כלורי נתרן ואשלגן הם חלק ממי הים.
מלח היה בשימוש על ידי אנשים מאז ימי קדם.נכון לעכשיו, השימוש בתרכובת בינארית זו אינו מוגבל לאכילה. אלקטרוליזה של תמיסה מימית של נתרן כלוריד מייצרת מתכת נתרן וגז כלור. מוצרים אלה משמשים בתהליכים תעשייתיים שונים כגון נתרן הידרוקסיד, מימן כלורי.
המשמעות של תרכובות בינאריות
קבוצה זו כוללת מספר רבחומרים, כך שנוכל לדבר בביטחון על היקף השימוש בהם בתחומים שונים של פעילות אנושית. אמוניה משמשת בתעשייה הכימית כמבשר לייצור חומצה חנקתית ובייצור דשנים מינרליים. זוהי תרכובת בינארית זו המשמשת בסינתזה אורגנית עדינה ומשמשת בקירור במשך זמן רב.
בשל הקשיות הייחודית של טונגסטן קרביד,תרכובת זו מצאה יישום בייצור של מגוון כלי חיתוך. האדישות הכימית של תרכובת בינארית זו מאפשרת להשתמש בה בסביבות אגרסיביות: ציוד מעבדה, תנורים.
"גז צחוק" (חנקן תחמוצת 1) מעורב בחמצן משמש ברפואה להרדמה כללית.
לכל התרכובות הבינאריות יש אופי קוולנטי או יוני של הקשר הכימי, סריג גביש מולקולרי, יוני או אטומי.

מסקנה
בעת הידור נוסחאות לתרכובות בינאריותיש צורך לעקוב אחר אלגוריתם מסוים של פעולות. היסוד המציג מצב חמצון חיובי (בעל ערך שליליות חשמלית נמוך יותר) נכתב ראשון. כאשר קובעים את הערך של מצב החמצון של היסוד השני, מספר הקבוצה שבה הוא נמצא מופחת משמונה. אם המספרים שהתקבלו שונים זה מזה, נקבעת הכפולה הפחות משותפת, ואז המדדים מחושבים.
בנוסף לתחמוצות, תרכובות אלה כוללותקרבידים, סיליקידים, פרוקסידים, הידרידים. אלומיניום וסידן קרבידים משמשים לייצור מעבדתי של מתאן ואצטילן, פרוקסידים משמשים בתעשייה הכימית כחומרי חמצון חזקים.
הליד כגון מימן פלואוריד (הידרופלואוריחומצה), המשמשת בהנדסת חשמל להלחמה. בין התרכובות הבינאריות החשובות ביותר, שבלעדיהם קשה לדמיין את קיומם של אורגניזמים חיים, המים נמצאים בראש. המאפיינים המבניים של תרכובת אנאורגנית זו נלמדים בפירוט בקורס הכימיה בבית הספר. זה על הדוגמה שלה שהחבר'ה מקבלים מושג על רצף הפעולות בעת הידור נוסחאות לתרכובות בינאריות.
לסיכום, נציין שקשה למצוא תחום כזה של תעשייה מודרנית, תחום של חיי אדם, בכל מקום שבו נעשה שימוש בתרכובות בינאריות שונות.