Az arének, amelyekhez a toluol tartozik, az ős és a homológ sorozat első tagjának, a benzolnak származékai. Az ebbe az osztályba tartozó vegyületek általános képlete CnX2n - 6... Az aromás szénhidrogének molekulái benzolgyűrűt (ciklust, magot) tartalmaznak. C toluol;7X8 tükrözi az anyag ehhez a nagyhoz való tartozásátszerves vegyületek egy csoportja. Sokan más néven ismerik a toluolt - metilbenzolt. Az anyagot széles körben használják az iparban, szerves oldószerként, folteltávolítóként és más célokra használják.
Mi a toluol?

Toluol kémiai képlete - C7X8 - másképp írható: C6X5–CH3. Ebben az esetben az atomok száma változatlan marad, de észrevehető különbség van a benzilhez képest, amelyet a metil gyök tartalmaz.
Más nómenklatúra-elveket alkalmazva a vegyületet metil-benzolnak és fenil-metánnak nevezik. Ez ugyanaz a toluol, amelynek általános képlete C7X8. De az első esetben a hangsúly azon vana benzolgyűrű szénatomjához kötődők egy hidrogénatomját metilcsoport helyettesíti. A második névnél más megközelítést alkalmaztak. Úgy gondolják, hogy a metánban az egyik hidrogént egy fenilcsoport helyettesíti. Ez az a részecske, amelyből a benzol hidrogénatomot ad át.
Molekuláris szerkezet

A metil-benzol szerkezeti képletei
A szénatomok közötti elektronikus sűrűség,amelyek az aromás magot alkotják, egyenletesen oszlanak el. A jelenség a benzol, a toluol és más aromás jelű (kör a gyűrűben) képletben tükröződik. Megjegyezzük egy metilcsoport jelenlétét is a mag egyik szénatomjánál. Az összes részecske közötti kapcsolatot kötőjelek mutatják. A szerkezeti képlet ebben az esetben az anyagmolekula összetételét és alapvető szerkezeti jellemzőit tükrözi.
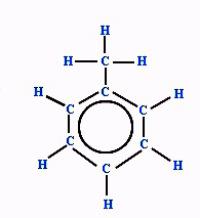
Egyszerűsített toluol-képlet - hatszögbelül kettős kötést mutató gyűrű. A metilcsoport a mag hat atomjának bármelyikén elhelyezkedhet, ekvivalensek egymással. Ennek a képmódnak a hátránya nyilvánvaló. A nyilvántartás nem ad képet az anyag összetételéről és a gyűrű összes szén-szén kötésének egyenértékűségéről.

Metilbenzol előállítás laboratóriumi és ipari célokra
A laboratóriumban először toluolt nyertek1835-1938 P. Peltier és A. Deville. Az első tudós fenyőgumit desztillált, a második pedig a kolumbiai Toluifera dél-amerikai fából kivont tolu balzsamot használta. Így keletkezett az anyag triviális neve - toluol. Jelenleg jelentős mennyiségű metilbenzolt állítanak elő olaj és kőszénkátrány desztillálásával, majd tisztítással. A kokszolási eljárás során toluolt extrahálnak a kokszoló kemence gázából. A sztirol szintézisében a benzol és az etilén reakciójának melléktermékeként szabadul fel. A laboratóriumban és az iparban a toluolt különböző módszerekkel nyerik.
- Aciklusos szénhidrogének dehidrociklizálása. A toluolt heptánból nyerik katalizátor jelenlétében 300 ° C hőmérsékleten.
- A benzol alkilezése, amelyet Friedel-Crafts reakciónak nevezünk. AlCl3 katalizátor vagy más katalizátor jelenlétében hajtják végre: С6H5–H + CH3Cl = C6H5–SN3 + HCl.
- Kölcsönhatás bróm-benzollal: C6H5–Br + CH3–Br + 2Na = С6H5–SN3 + 2NaBr.
- Cink és krezol keverése: C6X4B3OH + Zn = C6X5B3 + ZnO.
- Toluolszulfonsav feldolgozás.
A metilbenzol fizikai tulajdonságai

- A tiszta, színtelen folyadék festékillatot áraszt.
- A metilbenzol alacsony hőmérsékleten megszilárdul és –93 ° C-on olvadni kezd.
- A toluol forráspontja 110,63 ° C. Az anyag sűrűsége 0,8669 g / ml.
- A metil-benzol vízben való oldhatósága 20 ° C hőmérsékleten 0,47 g / l. Az M anyag (C7X8= 92,14 g / mol.
Toluol kémiai tulajdonságai: oxidáció
Az összes aréna jellemzőit kémiailag határozzák megstabil szénatom ciklus. A toluolképlet benzolgyűrű, amely formailag telítetlen, és metilcsoport. Az aromás szénhidrogének tulajdonságai hasonlóak az alkénekhez, amelyeket addíciós reakciók jellemeznek. De a benzol és homológjainak molekuláiban lévő hidrogénatomok részt vehetnek a szubsztitúciós reakciókban, ami közelebb hozza egymáshoz az arénákat és az alkánokat. A toluol reaktívabb, mint a benzol. Az anyagot oxidációs reakciók jellemzik.
- Égés szén-dioxid felszabadulásával és víz képződésével jár együtt: C7X8 + 9O2 = 7CO2 + 4H2O.
- Amikor a toluol kölcsönhatásba lép a kálium-permanganáttal, az anyagmolekula oldalláncában lévő metilcsoport karboxilvá oxidálódik. A reakció benzoesavat eredményez.
A toluol aromás magjának kémiai reakciói

- A metil-benzol-nitrálást keverékkel végezzüktömény salétrom- és kénsavakból áll. A toluolban található nitrocsoport elfoglalhatja az orto- és a para-helyzetet. A reakció az elektrofil szubsztitúció mechanizmusával megy végbe. Magas hőmérsékleten a trinitrotoluol (TNT) robbanóanyag képződik.
- A hidrogénezéssel egy hidrogénezéssel egy katalizátoron keresztül dezsromatizáláshoz és metil-ciklohexán: C7X8 + 3H2 = C7X14.
- Az erős hő- vagy UV-sugárzás mellett végzett klórozás hexaklór-ciklohexán képződését eredményezi.
Metilbenzol alkalmazások
A toluolt széles körben használják kiindulási anyagként a szerves szintézisben. Szükséges anyag sok anyag előállításához. Toluol alkalmazás:
- színezékek előállítása;
- folteltávolítók, mosószerek gyártása;
- TNT robbanóanyag előállítása;
- ragasztók, festékek, szintetikus illatanyagok és tisztítószerek használata oldószerként;
- festékek gyártása építési munkákhoz;
- Termékek kiadása körmökhöz;
- Gyógyszergyártás;
- az üzemanyag oktánszámának növelése;
- benzoesav, benzaldehid, benzil-klorid, szacharin, benzil-alkohol és más anyagok szerves szintézise;
A toluol iparként működikoldószer száraz tisztítószerekben, a bőr cserzéséhez használják. Számos kőolajtermék, fenol, formaldehid, növényvédő szerek és egyéb vegyületek elődje.

Toluol toxicitás
A metilbenzol gyúlékony anyag.A gőz-levegő keverék bizonyos körülmények között felrobban. A folyékony toluol nagyon gyúlékony. A szerkezeti képlet képet ad az összetételről és felépítésről, de nem tartalmaz információkat az anyag emberi testre gyakorolt hatásáról. Megállapították, hogy a toluol mérgező és rákkeltő hatású. A metilbenzol gőzök szabadon behatolnak a bőrbe, a légzőszervekbe, változásokat okoznak a központi idegrendszerben, az integumentáris szövetek irritációját, dermatitist okoznak. A toluolgőzök belélegzése esetén egy személy gátlást, remegést mutat, a vestibularis készülék aktivitása megszakad. Szükséges a toluollal, a festékekkel, az oldószerekkel gumikesztyűvel dolgozni, alaposan szellőztetni a szobát, vagy motorháztetőt használni. A metilbenzol egy gyenge kábítószer, amely toluol anyaggal való visszaélést okoz. Az anyag negatív hatásainak egyéb formái:

- szemirritáció és színlátás romlása;
- a hosszan tartó expozíció halláskárosodást okozhat;
- a magas vérkoncentráció májkárosodást, veseelhalást okoz;
- nagy mennyiségű gőz belélegzése szédüléshez, álmossághoz, fejfájáshoz vezet.
következtetés
A toluolt nagy mennyiségben állítják elő apetrolkémiai üzemekben vagy kokszgyárakban melléktermékként nyerték. A vegyület értékes alapanyag nagyszabású szerves szintézishez, és a gyógyszeriparban használják. A metil-benzolt sokféle oldószer tartalmazza, amelyeket festékekkel és lakkokkal végzett munkában használnak. A toluol a mérgező vegyületek osztályozásában a III. Veszélyességi osztályba tartozik. Ha egy anyaggal dolgozik, annak gőzkoncentrációja a levegőben nem haladhatja meg az egészségügyi és higiéniai előírások által meghatározott értékeket. Toluol kezelésekor nyílt lángot, szikrát nem szabad megengedni, ez robbanáshoz vezethet. A toluol légkörbe jutásával környezeti problémák is társulnak:
- olaj elégetésekor különböző típusú üzemanyagok;
- aktív vulkánokban;
- erdőtüzekben;
- oldószerek és festékek használatakor.
A toluol mérgező tulajdonságai, a tűz és a robbanás veszélye a folyékony anyag és gőzeinek gondos kezelését igényli.