I det periodiske system af Mendeleev på nummer 1placeret det mest almindelige element i universet - brint. Dens fordeling i procent er tæt på 75%. Dens laveste indhold bemærkes i atmosfærens lag - 0,0001%. Jordskorpen indeholder 1 vægtprocent gas. Dens største mængde findes i vand: 12%. Det er det tredje mest udbredte kemiske element på vores planet.
Varebeskrivelse
Brintmolekylet, hvis formel er H-H eller H2, er udstyret med fysiske og kemiske egenskaber.

Brint er en gas, der ikke er udstyret medfarve, ingen lugt. Placeringen af brint i tabellen på 1. plads skyldes, at dette element under forskellige forhold kan manifestere sig som et metal eller som en gas. I sin ydre orbital er der 1 elektron, som brint kan give (metalliske egenskaber) eller tage en anden (gaskvalitet).
Diameteren af et brintmolekyle er 27 nm.
Hydrogenatomets diameter er 1A, radius er 0,41 A.
egenskaber
Fysisk inkluderer følgende:
- Kogepunkt - 256cirkaS.
- Smeltepunkt -259,2cirkaS.
- Luftmasse (D) - 0,069.
- Brint er dårligt opløseligt i vand.
De kemiske egenskaber er som følger:
- Den ikke-polære binding mellem partiklerne i molekylet har en energi på 436 kJ / mol.
- Den termiske dissociationstemperatur er 2000cirkaS.
- Reagerer med:
- halogener;
- ilt;
- grå;
- nitrogen;
- nitrogenoxid;
- aktive metaller.
Under naturlige forhold forekommer brint både naturligt og i form af isotoper: protium, deuterium og tritium.
Strukturen af molekylet
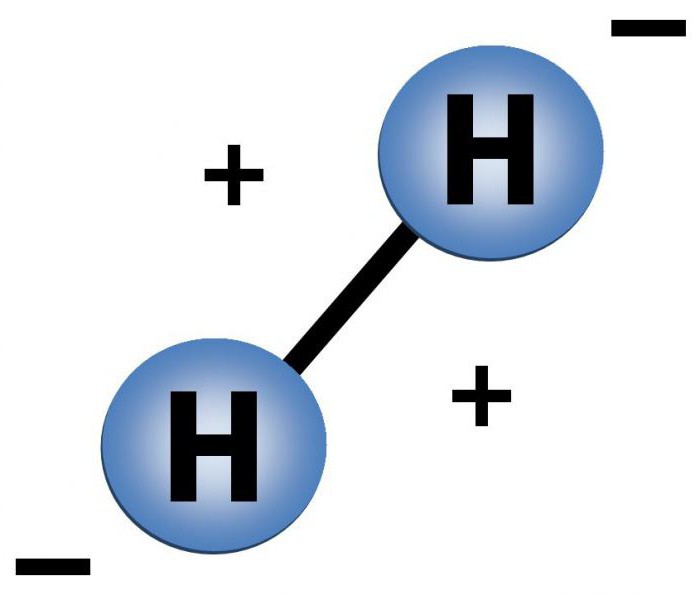
Elementets molekyle har en enkel struktur.Sammensætningen af hydrogenmolekylet er repræsenteret af to atomer, der nærmer sig danner en kovalent ikke-polær binding såvel som et elektronpar. Strukturen af et atom er: 1 positivt ladet kerne, omkring hvilken 1 negativt ladet elektron bevæger sig. Denne elektron er placeret i 1s orbital.
H - 1e = H + denne hydrogenion er positiv.
Dette udtryk indikerer, at brinthar lignende parametre som elementerne i gruppe 1 i det periodiske system, som er alkalimetaller (lithium, natrium, kalium), der donerer deres eneste elektron i den ydre orbital.
Н + 1е = Н– negativ hydrogenion.
Denne ligning viser, at brint errelateret til lignende elementer fra den 7. gruppe, som er gas og er i stand til at modtage manglende elektroner til deres ydre elektroniske niveau. Disse gasser inkluderer: fluor, klor, brom osv.
Sammensætningen af hydrogenmolekylet er vist grafisk nedenfor.

Afstand mellem hydrogenatomer r = 0,74 A, cmens summen af orbitale radier er 1.06 A. Dette påvirker elektronskyernes overlapningsdybde og den stærke, stabile hydrogenbinding.
Hydrogenatomet er det mest elementære atom i naturen. Atomprotonens størrelse er 10,5 A, og diameteren på et atom er 0,1 nm.
Isotopmolekyler har en speciel struktur. Atomkernen i protium består kun af en proton. Isotopen er betegnet: 1H.
Den nukleare struktur ligner et kompleks af en proton og en neutron (2H).
3H - tritium - i sin atomstruktur er udstyret med en kerne med 1 proton og to neutroner.
Vægt
I videnskaben er der formler, der beregner massen af et brintmolekyle. I forhold til elementet bestemmes molekyl- og atomvægten.

Den molære masse af et brintmolekyle beregnes ved hjælp af den generelle formel:
M = m / n, hvor m er stoffets masse, n er dets mængde.
Atommassen er 1.008 amu.Derfor vil molekylets relative masse også være lig med 1,008. Da et brintmolekyle består af to atomer, er den relative atomvægt 2,016 amu. e. m. Massen af et brintmolekyle udtrykkes i gram pr. mol (g / mol).
Værdi i naturen

Det mest betydningsfulde stof i naturen, der danner brint i et kompleks med ilt, er vand. Vand er kilden til liv, derfor er brint et vigtigt element.
Af 100% af alle kemiske grundstoffer, derudgør det organismiske miljø, 1/10 del eller 10%, er brint. Ud over vand er det i stand til at opretholde en kvaternær proteinstruktur, hvilket er muligt på grund af hydrogenbinding.
Princippet om komplementaritet af nukleinsyrerforekommer også med virkningen af et brintmolekyle. I en plantecelle deltager H i processen med fotosyntese, biosyntese og i overførsel af energi gennem membrankanaler.
ansøgning
Brint anvendes i vid udstrækning i den kemiske industri. Det tilsættes til fremstilling af plastprodukter, til sæbefremstilling samt til ammoniak- og mentholproduktion.
Fødevareindustri:i fødevareproduktion tilsættes brint som et fødevaretilsætningsstof E949. En sådan komponent kan ses på emballagen af margarine, vegetabilske olier. E949-tilsætningsstof er godkendt af Den Russiske Føderations fødevareindustri.
Brint blev engang brugt iluftfartsindustrien, fordi stoffet er lettere end luft. Så i 30'erne af det sidste århundrede blev balloner og luftskibe fyldt med denne type gas. På trods af de lave omkostninger og brugervenlighed ophørte brint snart med at blive brugt som fyldstof, da tilfælde af flyeksplosioner blev hyppigere.
Gas bruges i dag som brændstofanvendt i rumfartsindustrien. Imidlertid overvejes metoder til at bruge det til drift af motorer til biler og lastbiler, da elementet under forbrænding ikke udsender skadelige urenheder i atmosfæren og derfor er miljøvenligt.
En integreret komponent af brintisotoperfungere som en del af mange medikamenter. Deuterium bruges i farmakologisk forskning til at bestemme opførslen og virkningerne af et lægemiddel i kroppen. Tritium bruges i radiodiagnostik som et element, der bestemmer de biokemiske reaktioner ved enzymmetabolisme. Brint er en del af peroxidet, som er et desinfektionsmiddel.






