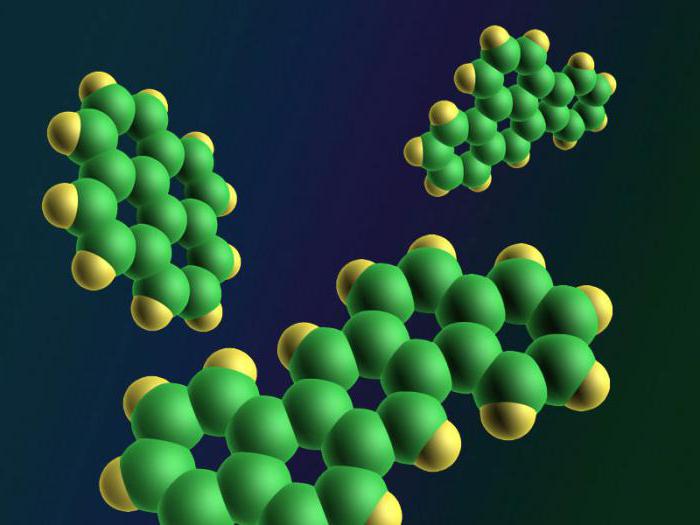
Съединение като бензол, г-жа Химия вфермата му окончателно и безвъзвратно се сдобива едва през 1833г. Бензолът е съединение с краткотраен, може дори да се каже експлозивен характер. Как разбрахте?
история
Йохан Глаубер през 1649 г. насочи вниманието си към съединението, което успешно се формира, когато химикът се занимава с преработка на въглен катран. Но тя пожела да остане инкогнито.
След около 170 години и да бъдем много повечеточно, в средата на двадесетте години на XIX век случайно бензинът се извлича от газа на газа, а именно от отделения кондензат. Човечеството дължи такива усилия на Майкъл Фарадей, учен от Англия.
Германец прихвана релето бензолЕйгард Микерлич. Това се случи, когато се проведе процесът на лечение на безводни калциеви соли на бензоена киселина. Може би затова съединението получи името бензен. Все пак като опция ученият го нарече бензин. Тамян, ако е преведен от арабски.
Бензолът изгаря красиво и ярко, във връзка с тези наблюдения Огюст Лоран го посъветва да го нарече "сешоар" или "бензол". Ярки, блестящи - ако са преведени от гръцки.

Въз основа на мнението на Линус Полинг, концепцията заестеството на електронната комуникация, относно качествата на бензола, ученият предостави молекулата на съединението под формата на следното изображение. Това е шестоъгълник. В него е вписан кръг. Горното показва, че бензолът има интегрален електронен облак, който безопасно съдържа шест (без изключение) въглеродни атоми на цикъла. Облигационните бинарни връзки не се наблюдават.
Те работеха с бензол като разтворител.Но по принцип, както се казва, не е бил член, не е участвал, не е участвал. Но това е през 19 век. През XX имаше значителни промени. Свойствата на бензола изразяват най-ценните качества, които му помогнаха да стане по-популярен. Октановото число, което се оказа високо, направи възможно използването му като горивен елемент за зареждане на автомобили. Това действие послужи като тласък за широкото изземване на бензола, извличането на който се осъществява като вторичен продукт от производството на коксуваща стомана.
До четиридесетте години в химическата област бензолът е започналконсумиран при производството на вещества, които бързо се взривяват. 20 век се увенчава с факта, че нефтопреработващата промишленост произвежда толкова много бензол, че започва да доставя химическата промишленост.
Характеристика на бензола
Ненаситените въглеводороди са много подобни на бензола.Например, въглеводородната серия от етилен се характеризира като ненаситен въглеводород. Той се характеризира с реакция на присъединяване. Бензолът лесно претърпява реакция на заместване. Всичко това е благодарение на атомите, които са в една и съща равнина. И като факт - конюгиран облак от електрон.

Ако във формулата присъства бензолен пръстен, това означава, че можем да стигнем до елементарното заключение, че това е бензол, структурната формула на който изглежда точно така.
Физични свойства
Бензолът е течност, която няма цвят,но има съжаляваща миризма. Бензолът се топи, когато температурата достигне 5,52 градуса по Целзий. Кипва при 80.1. Плътността е 0,879 g / cm3, моларната маса е 78,11 g / mol.При изгаряне много пуши. Образува взривни съединения, когато навлиза въздух. Органичните разредители (бензин, етер и други) с описаното вещество се комбинират без проблеми. Азеотропното съединение създава с вода. Загряването преди изпаряването започва при 69,25 градуса (91% бензол). При 25 градуса по Целзий може да се разтвори във вода 1,79 g / l.
Химични свойства
Бензолът реагира със сярна и азотна киселина.А също и с алкени, халогени, хлоралани. Реакцията на заместване е това, което е характерно за него. Температурата на налягането влияе на пробива на бензолния пръстен, който се осъществява при доста тежки условия.
Всяко уравнение на реакцията на бензен може да бъде разгледано по-подробно.
1. Електрофилно заместване. Бромът, в присъствието на катализатор, взаимодейства с хлора. В резултат на това получаваме хлоробензен:
C6H6 + 3Cl2 → C6H5Cl + HCl
2. Реакция на Фридел-Крафтс или алкилиране с бензен. Появата на алкилбензоли се дължи на комбинацията с алкани, които са халогенирани:
C6H6 + C2H5Br → C6H5C2H5 + HBr
3. Електрофилно заместване. Тук се провеждат реакциите на нитриране и сулфонация. Уравнението на бензола ще изглежда така:
C6H6 + H2SO4 → C6H5SO3H + H2O
C6H6 + HNO3 → C6H5NO2 + H2O
4. Бензен по време на горенето:
2C6H6 + 15O2 → 12CO2 + 6H2O
При определени условия той проявява характер, характерен за наситените въглеводороди. P-електронният облак, който е в структурата на разглежданото вещество, обяснява тези реакции.
Различните видове бензен зависят от специалната технология.От тук идва етикетирането на петролен бензол. Например, пречистен и силно пречистен за синтез. Бих искал да отбележа отделно хомолозите на бензола и по-точно техните химични свойства. Това са алкилбензоли.

Хомолозите на бензола са много по-отзивчиви. Но гореспоменатите реакции на бензола, а именно хомолозите, протичат с известна разлика.
Халогениране на алкилбензоли
Уравнението е както следва:
C6H5-CH3 + Br = C6H5-CH2Br + HBr.
Тенденцията на брома към бензолния пръстен не се наблюдава. Излиза на верига отстрани. Но благодарение на катализатора за солта Al (+3) бромът отива смело в пръстена.
Нитриране на алкилбензоли
Благодарение на сярната и азотната киселини те се нитриратбензоли и алкилбензоли. Реактивни алкилбензоли. Получават се два продукта от трите представени - това са пара- и ортоизомери. Можете да напишете една от формулите:
C6H5 - CH3 + 3HNO3 → C6H2CH3 (NO2) 3.
Окисление
Това е неприемливо за бензола. Но алкилбензолите реагират лесно. Например бензоена киселина. Формулата е показана по-долу:
C6H5CH3 + [O] → C6H5COOH.
Алкилбензен и бензен, тяхното хидрогениране
В присъствието на усилвател започва водородътвзаимодействат с бензен, което води до образуването на циклохексан, както беше споменато по-горе. Алкибензолите също се превръщат в алкилциклохексани без проблем. За да се получи алкилциклохексан, желаният алкилбензен трябва да се хидрира. По принцип това е необходима процедура за производството на чист продукт. И това не са всички реакции на бензола и алкилбензола.
Производство на бензен. Промишленост
Основата на такова производство се основава наза обработка на компоненти: толуен, нафта, смола, която се отделя при крекинг на въглища и други. Следователно бензенът се произвежда в нефтохимически и металургични предприятия. Важно е да знаете как да получите бензол с различна степен на пречистване, тъй като марката на това вещество е пряко зависима от принципа на производство и предназначението.
Лъвският дял се получава чрез термокаталитично риформиране на каустобиолитната част, кипене при 65 градуса, с ефект на екстракт, дестилация с диметилформамид.
При производството на етилен и пропилен се получава течностпродукти, които се образуват при разлагането на неорганични и органични съединения под въздействието на топлина. Бензолът също е изолиран от тях. Но, за съжаление, няма толкова много изходни материали за този вариант на производство на бензен. Следователно веществото от интерес за нас се извлича чрез реформиране. По този метод се увеличава обемът на бензола.

Чрез деалкилиране при температура 610-830градуса със знак плюс, в присъствието на пара, генерирана от кипене на вода и водород, бензен се получава от толуен. Има и друг вариант - каталитичен. Когато се наблюдава наличието на зеолити или, като опция, оксидни катализатори, при температурен режим от 227-627 градуса.
Има и друг, по-стар начинразработване на бензен. С помощта на абсорбция от абсорбери с органичен произход, той се отделя от крайния резултат от коксуването на въглища. Продуктът е парогазов и предварително охладен. Например използва се нефт, чийто източник е нефт или въглища. Когато дестилацията се извършва с пара, чистачът се отделя. Хидроочистването помага за освобождаването на суровия бензен от излишните вещества.
Въглищни суровини
В металургията при използване на въглища иако се уточни - сухата му дестилация, вземете кокс. По време на тази процедура въздушният поток е ограничен. Не забравяйте, че въглищата се загряват до температура 1200-1500 по Целзий.
Химическият бензен за въглища се нуждае задълбоченопрочистване. Наложително е да се отървете от циклохексан метил и неговия другар n-хептан. Наситените въглеводороди също трябва да бъдат отстранени. Бензенът е изправен пред процес на разделяне и пречистване, който ще се извършва повече от веднъж.
Методът, описан по-горе, е най-старият, но с течение на времето той губи високите си позиции.
Маслени фракции
0,3-1,2% - такива показатели за състава на нашия геройв суров нефт. Оскъдни показатели за инвестиране на пари и усилия. Най-добре е да се използва промишлен процес за преработка на петролни фракции. Тоест каталитично реформиране. В присъствието на алуминиево-платинено-рениев усилвател процентът на съдържанието на ароматни въглехидрати се увеличава и се увеличава показател, който определя способността на горивото да не се самозапали по време на компресията.
Пиролизни смоли
Ако извлечем нашия петролен продукт от нетвърдо веществосуровини, а именно чрез пиролиза, произтичаща от производството на пропилен и етилен, тогава този подход ще бъде най-приемлив. За да бъдем точни, бензенът се отделя от пирокондензат. Разлагането на определени фракции изисква хидрообработка. Сяра и ненаситени смеси се отстраняват по време на почистването. Първоначалният резултат показва съдържанието на ксилол, толуен, бензен. С помощта на извличане, което е свръхактивно, BTK групата се отделя и се получава бензен.
Хидродеалкилиране на толуен
Главните герои на процеса, водороден коктейлпотокът и толуенът се подават загряти в реактора. Толуенът преминава през слоя на катализатора. По време на този процес метиловата група се отделя, за да образува бензен. Тук е подходящ определен метод на пречистване. Резултатът е високо чисто вещество (за нитриране).
Непропорционалност на толуола
Поради отхвърлянето на метиловия классъздава се бензен, ксилолът се окислява. В този процес се забелязва трансалкилиране. Каталитичното действие се дължи на паладия, платината и неодима, намиращи се върху алуминиевия триоксид.
В реактор със стабилен слой на катализатораподават се талуен и водород. Целта му е да предотврати утаяването на въглеводородите в равнината на катализатора. Потокът, който напуска реактора, се охлажда и водородът се възстановява безопасно за рециклиране. Това, което е останало, се дестилира три пъти. В началния етап съединенията, които не са ароматни, се изтеглят. Вторият е бензен, а последната стъпка е екстракцията на ксилоли.
Тримеризация на ацетилен
Благодарение на трудовете на френския физик-химикМарцелена Бертлот започва да произвежда бензен от ацетилен. Но в същото време тежък коктейл се открояваше от много други елементи. Въпросът беше как да се намали температурата на реакцията. Отговорът е получен едва в края на четиридесетте години на XX век. В. Репе намери подходящия катализатор, оказа се, че е никел. Тримеризацията е единственият начин да се получи бензол от ацетилен.

Бензенът се образува с помощта наактивен въглен. При високи индекси на топлина ацетиленът преминава през въглищата. Бензенът се отделя, ако температурата е най-малко 410 градуса. В същото време все още се раждат разнообразни ароматни въглеводороди. Следователно е необходимо добро оборудване, което е способно за висококачествено пречистване на ацетилен. С такъв трудоемък метод като тримеризация се консумира много ацетилен. За да се получат 15 ml бензен, се вземат 20 литра ацетилен. Можете да видите как изглежда във формулата (ацетилен-бензен), реакцията няма да отнеме много време.
3C2H2 → C6H6 (уравнение на Зелински).
3CH → CH = (t, kat) = C6H6.
Къде се използва бензен
Бензенът е доста популярно въображение на химията.Особено често се забелязва как бензенът се възприема при производството на кумен, циклохексан, етилбензен. За да се създаде стирен, етилбензолът е незаменим. Изходният материал за производството на капролактам е циклохексан. Когато се прави термопластична смола, се използва именно капролактам. Описаното вещество е незаменимо при производството на различни бои, лакове.
Колко опасен е бензолът
Бензенът е токсично вещество.Проявата на чувство на неразположение, което е придружено от гадене и силно замайване, е признак на отравяне. Дори летален изход не е изключен. Усещането за неописуема наслада е не по-малко тревожните камбани в случай на отравяне с бензен.
Течният бензен е дразнещкожата. Бензоловите пари лесно проникват дори през непокътната кожа. При най-краткосрочен контакт с вещество в малка доза, но редовно неприятните последици няма да отнемат много време. Това може да бъде увреждане на костния мозък и остра левкемия от различни видове.

Освен това веществото води до пристрастяванечовек. Бензенът действа като дрога. Катранен продукт се получава от тютюнев дим. Когато го проучиха, стигнаха до заключението, че съдържанието на последното не е безопасно за хората. В допълнение към наличието на никотин е установено и присъствието на ароматни въглехидрати от бензпиреновия тип. Отличителна черта на бензпирена са канцерогенните вещества. Те имат много вредно въздействие. Например те причиняват рак.
Независимо от горното, бензенът еизходна суровина за производството на различни лекарства, пластмаси, синтетичен каучук и, разбира се, багрила. Това е най-разпространеното въображение на химията и ароматно съединение.