De eenvoudigste meerwaardige alcohol waariner zijn 3 OH-groepen, - glycerine. De gemeenschappelijke formule voor verbindingen van dit type is CnH2n - 1 (OH) 3. Om een beter begrip te krijgen van de eigenschappen en het gebruik van glycerol en zijn homologen, moet u de variëteiten van de formules van stoffen overwegen, die elk in bepaalde situaties worden gebruikt.
Classificatie en nomenclatuur van glycerolen
In de organische chemie zijn alcoholen stoffenderivaten van koolwaterstoffen. Sommige waterstofatomen in de moleculen zijn vervangen door een of meer hydroxygroepen. Alcoholen verschillen in het aantal OH-groepen (een-, twee-, polyatomisch). De laagste vertegenwoordigers van de klasse met het aantal koolstofatomen van 1 tot 12 zijn vloeibare stoffen, de hogere zijn vaste stoffen. Alcantriolen of glycerolen zijn driewaardige alcoholen die drie hydroxylgroepen bevatten die zijn gebonden aan drie verschillende koolstofatomen. Verbindingen die tot deze groep behoren, vertonen amfotere eigenschappen vanwege de wederzijdse invloed van de hydroxygroep en de radicaal.

De eenvoudigste vertegenwoordiger van alkanthriols is propaantriol-1,2,3 (synoniem - glycerol). Formule van de stof - C.3X8oh3... Systematische nomenclatuur suggereertvermelding van de naam van de corresponderende alkaan met het woord "triol", het gebruik van Arabische cijfers die de positie van de OH-groep aangeven. De nummering in de moleculen van glycerolhomologen is van de hydroxylgroep die zich het dichtst bij het einde van de keten bevindt. Mogelijke soorten isomerie: structuur van de koolstofketen, positie van hydroxygroepen, optisch.
Ontdekking van glycerine
In 1779 kreeg de Zweedse apotheker K. Scheele voor het eerst een nieuwe stroperige stof bij het verzepen van vetten. 33 jaar later noemde de Fransman M. Chevreul de zoete vloeibare glycerine.
De chemische samenstelling werd in 1836 door Peluz vastgesteld.Berthelot (1854) en Würz (1857), die glycerine bleven bestuderen, leverden een belangrijke bijdrage aan de studie van de structuur. De moleculaire formule en de aard van de radicaal maakten het mogelijk om glycerine als beperkende alcoholen te classificeren.
De behoefte aan glycerine is aanzienlijk toegenomenna 1847, toen de salpeterzuurester werd ontdekt. In 1875 slaagde de Zweedse ingenieur A. Nobel erin om explosieven te verkrijgen - dynamiet met behulp van glycerine.
Samenstelling, structuur en eenvoudigste formule van glycerine
De eenvoudigste beschrijving van de samenstelling van een stof valt samen met de ware, empirische en grove formule van glycerine - C3X8oh3... De koolstofketen heeft 3 atomen, elk vandeze zijn gekoppeld aan een hydroxygroep. De atomen waaruit de stof bestaat, worden aangeduid met chemische symbolen: C - koolstof, O - zuurstof, H - waterstof. De samenstelling van glycerine weerspiegelt verschillende formules (moleculair, structureel). Kogelstang- en halfronde modellen worden veel gebruikt bij de studie van materie. Computer-gegenereerde 2D- en 3D-structuren zijn ruimtelijke weergaven van een glycerolmolecuul. Ze maken het mogelijk om de compositie, onderlinge rangschikking en afstand, de bindingshoek tussen atomen te visualiseren.

Moleculaire en molaire massa van glycerol
Volgens de formule kun je de moleculaire en molaire waarde vindenmassa, percentage elementen in de stof. Voor berekeningen is het noodzakelijk om de waarden van de atoommassa's van de elementen aangegeven in het periodiek systeem te gebruiken. Empirische formule van glycerine: C.3X5(OH)3... Door de atomaire massa te vermenigvuldigen (in amu.) van elk element door het aantal atomen met de daaropvolgende toevoeging van de verkregen waarden, vinden we de moleculaire (Mr) en molaire (M) massa's. Voor dit type berekening is het handiger om de brutoformule van glycerine - C te gebruiken3X8oh3.
- Ar (H) = 1,00794; het aantal atomen in een molecuul is 8.
- Ar (C) = 12,0107; atomen - 3.
- Ar (O) = 15,9994; atomen - 3.
- De heer (C3H8oh3) = 12.0107 * 3 + 1.00794 * 8 + 15.9994 * 3 = 92.09382 a. eten.
- M (C3H8oh3) = 92,09382 g / mol /
- Het percentage elementen in een molecuul van een stof: H - 8,756%, C - 39,125%, O - 52,119%.

Rationele en structurele formule van glycerine
De samenstelling van de stof en zijn moleculen weerspiegelenrationele en grove formule, maar ze geven geen idee van de rangschikking van atomen die glycerine onderscheiden. De structuurformule en het computermodel zijn beter geschikt om de structuur van een molecuul, de bindingen tussen atomen, te bestuderen.
- Rationele glycerine-formule - C.3X5(OH)3 ... Uit de samenstelling van het molecuul worden de functionele OH-groepen geïsoleerd en tussen haakjes ingesloten. Direct na het sluitende haakje staat het aantal hydroxygroepen in het molecuul.
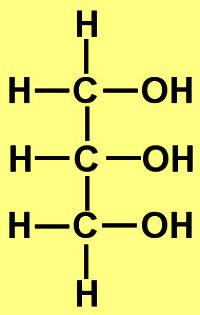
- Semi-uitgebreide rationele formule - HOCH2CH (OH) CH2OH (glycerine).
- De structuurformule geeft grafisch de locatie van het molecuul weer. Streepjes tussen atomen symboliseren chemische bindingen.
- De Lewis-structuur bevat stippen die valentie-elektronen vertegenwoordigen en paren die betrokken zijn bij de vorming van bindingen.
Sommige soorten afbeeldingen van een molecuul nemen veel ruimte in beslag, dus gebruiken ze vaak verkorte formules, bijvoorbeeld HOCH2—SNON - CH2OH, evenals skeletstructuren:

De toestand van atomen in het glycerinemolecuul
Hydroxyl is een polair deeltje, naast zuurstofbezit een eenzaam paar elektronen. De aanwezigheid van drie hydroxygroepen leidt tot verdere polarisatie van de OH-binding. Een gedeeltelijke lading "+" verschijnt op de koolstofatomen, waardoor de nucleofiele substitutie van de hydroxylgroep wordt vergemakkelijkt. De kenmerken van de samenstelling en structuur, die worden weerspiegeld door de structuurformule van glycerine, worden bevestigd in de eigenschappen van de stof. Deze verbinding wordt gekenmerkt door talrijke waterstofbruggen - zwakke extra bindingen. Glycerine heeft meer uitgesproken zure eigenschappen in vergelijking met ethanol en propanol. De belangrijkste derivaten zijn onder meer glyceroltrioleaat. Formule:
- de eenvoudigste - C57H104oh6;
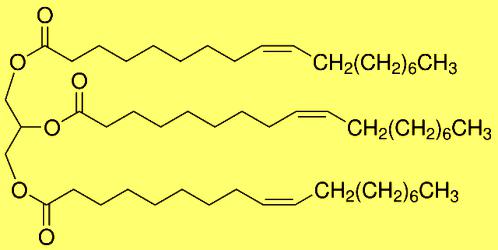
- semi-geëxpandeerd rationeel - (С17H33SOO)3C3H5;
- rationeel met structurele en skeletelementen -
Glycerine uiterlijk
Bij kamertemperatuur, propaantriol-1,2,3 -kleurloze of lichtgele vloeistof, reukloos, zoet van smaak. Glycerine, uitgehard bij lage temperaturen, smelt bij een temperatuur van 17,8 ° C. Het koken van de stof, gevolgd door verdamping, begint bij 290 ° C. Glycerine is iets zwaarder dan water, de dichtheid wordt berekend bij 20 ° C en geeft een waarde van 1,2604 g / cm3.

Eigenschappen van propaantriol-1,2,3
De chemische formule van glycerine geeft nietideeën over de amfotere aard van de compound. Zwakke zure en basische eigenschappen van stoffen worden geassocieerd met de eigenaardigheden van de invloed van atomen in het molecuul, polarisatie in de O - H-groep. In aanwezigheid van alkali, interageert glycerine met koper (II) hydroxide, wat resulteert in een complex gekleurd blauw (een van de kwalitatieve reacties). Met zuren eindigt de reactie van glycerine met de vorming van esters. Wisselwerking van driewaardige alcohol met salpeterzuur in aanwezigheid van H.2Met4 (conc.) leidt tot de vorming van nitroglycerine.
Thuis van vetten en oliën gebruikenglycerine, ethylalcohol en andere ingrediënten krijgen zeep. Het kookproces vereist een zorgvuldige verwarming van de massa in een waterbad, een creatieve houding ten opzichte van de selectie van componenten en vormen voor het afgewerkte zeepproduct.
Glycerine en zijn derivaten worden gebruikt in email,verven, veel medicijnen, toiletartikelen. Het bevat een zoete substantie in een breed scala aan voedingsmiddelen, waaronder gebakken goederen. De internationale naam voor een zoetstof en smaakstof voor zoetwaren is E422. Samen met andere alcoholen en vetzuuresters wordt glycerine gezien als een mogelijke vervanging voor van aardolie afgeleide brandstoffen. Zuinige methoden voor het gebruik van nieuwe soorten biodiesel voor het tanken van auto's zullen een revolutie teweegbrengen in de wereldwijde transportsector. De ecologische situatie zal aanzienlijk verbeteren en de afhankelijkheid van de wereldeconomie van olie- en gaswinning zal afnemen.