Antes de analizar cómo componer isómeros de hidrocarburos saturados, identifiquemos las características de esta clase de sustancias orgánicas.
Hidrocarburos saturados
En química orgánica, se distinguen muchas clasesCxHy. Cada uno tiene su propia fórmula general, series homólogas, reacciones cualitativas y aplicación. Los hidrocarburos saturados de la clase de alcanos se caracterizan por enlaces sencillos (sigma). La fórmula general para esta clase de sustancias orgánicas es CnH2n + 2. Esto explica las principales propiedades químicas: sustitución, combustión, oxidación. La unión no es típica de las parafinas, ya que los enlaces en las moléculas de estos hidrocarburos son simples.

Isomería
Un fenómeno como el isomería explicavariedad de sustancias orgánicas. Por isomería, se acostumbra entender el fenómeno en el que existen varios compuestos orgánicos que tienen la misma composición cuantitativa (el número de átomos en una molécula), pero su disposición diferente en la molécula. Las sustancias resultantes se denominan isómeros. Pueden ser representantes de varias clases de hidrocarburos y, por lo tanto, difieren en propiedades químicas. Un compuesto diferente en la molécula de alcano de los átomos de C conduce a la aparición de isomería estructural. ¿Cómo hacer isómeros de alcanos? Existe un cierto algoritmo según el cual es posible representar los isómeros estructurales de una clase determinada de sustancias orgánicas. Una posibilidad similar aparece solo a partir de cuatro átomos de carbono, es decir, de la molécula de butano C4H10.
Variedades de isomería
Entender cómo escribir fórmulas.isómeros, es importante tener una idea de sus tipos. Si hay átomos idénticos dentro de la molécula en igual número, ubicados en el espacio en un orden diferente, estamos hablando de isomería espacial. De lo contrario, se llama estereoisomería. En tal situación, el uso de fórmulas estructurales por sí solo no será suficiente, se requerirá el uso de fórmulas especiales de proyección o espaciales. Los hidrocarburos saturados, comenzando con H3C - CH3 (etano), tienen diferentes configuraciones espaciales. Esto se debe a la rotación dentro de la molécula a lo largo del enlace C-C. Es un enlace σ simple que crea isomería conformacional (rotacional).

Isomería estructural de parafinas
Hablemos de cómo hacer isómeros de alcanos.La clase tiene isomería estructural, es decir, el átomo de carbono forma cadenas diferentes. De lo contrario, la posibilidad de cambiar la posición en la cadena de átomos de carbono se denomina isomería del esqueleto carbónico.

Isómeros de heptano
Entonces, cómo dejar isómeros para una sustancia,que tiene la composición C7H16? Para empezar, puede organizar todos los átomos de carbono en una cadena larga, agregue para cada uno un cierto número de átomos de C. ¿Cuántos? Dado que la valencia del carbono es cuatro, los átomos más externos tendrán tres átomos de hidrógeno y los internos tendrán dos. La molécula resultante tiene una estructura lineal, tal hidrocarburo se llama n - heptano. La letra "n" implica un esqueleto de carbono directo en un hidrocarburo dado.
Ahora cambiamos la disposición de los átomos de carbono,Mientras se "acorta" la cadena de carbono lineal en C7H16. Los isómeros pueden estar compuestos en forma estructural expandida o abreviada. Consideremos la segunda opción. Primero, colocamos un átomo de C en forma de radical metilo en diferentes posiciones.
Este isómero de heptano tiene el siguiente nombre químico: 2-metilhexano. Ahora "movemos" el radical al siguiente átomo de carbono. El hidrocarburo saturado resultante se llama 3-metilhexano.
Si movemos el radical más lejos,la numeración comenzará por el lado derecho (el radical hidrocarbonado se encuentra más cerca del inicio), es decir, obtendremos el isómero que ya tenemos. Por lo tanto, pensando en cómo componer fórmulas de isómeros para la sustancia inicial, intentaremos hacer el esqueleto aún "más corto".
Los dos carbonos restantes se pueden representar como dos radicales libres: metilo.
Primero coloquémoslos en diferentes carbonos en la cadena principal. Llamemos al isómero obtenido -2,3 dimetilpentano.
Ahora dejemos un radical en el mismo lugar y transfiramos el segundo al siguiente átomo de carbono de la cadena principal. Esta sustancia se llama 2,4 dimetilpentano.
Ahora organicemos los radicales de hidrocarburos en un átomo de carbono. Primero, para el segundo, obtenemos 2,2 dimetilpentano. Luego, en el tercero, habiendo recibido 3,3 dimetilpentano.
Ahora dejamos cuatro átomos en la cadena principal.carbono, los tres restantes se utilizan como radicales metilo. Los ordenamos de la siguiente manera: dos en el segundo átomo de C, uno en el tercer carbono. Llamamos al isómero resultante: 2,2,3 trimetilbutano.
Usando el heptano como ejemplo, hemos discutido cómo componer correctamente los isómeros de los hidrocarburos saturados. La foto muestra ejemplos de isómeros estructurales para el buteno6 de sus derivados de cloro.

Alquenos
Esta clase de sustancias orgánicas tiene un comúnla fórmula CnH2n. Además de los enlaces C-C saturados, esta clase también contiene un doble enlace. Es ella quien determina las principales propiedades de esta serie. Hablemos de cómo dejar los isómeros de los alquenos. Intentemos identificar sus diferencias con los hidrocarburos saturados. Además de la isomería de la cadena principal (fórmulas estructurales), los representantes de esta clase de hidrocarburos orgánicos también se caracterizan por tres tipos más de isómeros: geométricos (cis y transformada), múltiples posiciones de enlace e isomería entre clases (con cicloalcanos).

Isómeros C6H12
Intentemos averiguar cómo componer los isómeros c6h12, teniendo en cuenta el hecho de que una sustancia con esta fórmula puede pertenecer a dos clases de sustancias orgánicas a la vez: alquenos, cicloalcanos.
Primero, pensemos en cómo hacer isómeros.alquenos si hay un doble enlace en la molécula. Ponemos una cadena de carbono recta, ponemos un enlace múltiple después del primer átomo de carbono. Intentemos no solo componer los isómeros de С6Н12, sino también nombrar las sustancias. Esta sustancia es hexeno - 1. El número indica la posición en la molécula del doble enlace. Cuando se mueve a lo largo de la cadena de carbono, obtenemos hexeno -2, así como hexeno-3.
Ahora pensemos en cómo hacer isómeros para esta fórmula cambiando el número de átomos en la cadena principal.
Primero, acortemos el esqueleto de carbono en uno.átomo de carbono, se considerará un radical metilo. Dejaremos el doble enlace después del primer átomo de C. De acuerdo con la nomenclatura sistemática, el isómero resultante tendrá el siguiente nombre: 2 metilpenteno - 1. Ahora movemos el radical hidrocarburo a lo largo de la cadena principal, dejando la posición del doble enlace. sin alterar. Este hidrocarburo insaturado ramificado se denomina 3 metilpenteno -1.
Es posible un isómero más sin cambiar la cadena principal y la posición del doble enlace: 4 metilpenteno -1.
Para la composición C6H12, puede intentar moverun doble enlace de la primera a la segunda posición, sin transformar la propia cadena principal. En este caso, el radical se moverá a lo largo del esqueleto carbónico, comenzando desde el segundo átomo de C. Este isómero se llama 2 metilpenteno-2. Además, puede colocar el radical CH3 del tercer átomo de carbono, obteniendo así 3 metilpenteno-2
Si se coloca un radical en el cuarto carbono de un átomo de esta cadena, se formará otra nueva sustancia de hidrocarburo insaturado con un esqueleto de carbono sinuoso: 4 metilpenteno-2.
Con una mayor reducción del número de C en la cadena principal, puede obtener otro isómero.
Dejamos el doble enlace después del primer átomo de carbono y colocamos dos radicales en el tercer átomo de C de la cadena principal, obtenemos 3.3 dimetilluteno-1.
Ahora pongamos radicales en el carbono vecinoátomos, sin cambiar la posición del doble enlace, obtenemos 2,3 dimetilbuteno-1. Intentemos, sin cambiar el tamaño de la cadena principal, mover el doble enlace a la segunda posición. En este caso, podemos suministrar radicales solo a 2 y 3 átomos de C, habiendo obtenido 2,3 dimetilbuteno-2.
No existen otros isómeros estructurales para este alqueno, cualquier intento de inventarlos conducirá a una violación de la teoría de AM Butlerov sobre la estructura de las sustancias orgánicas.

Isómeros espaciales de C6H12
Ahora descubramos cómo componer isómeros y homólogos en términos de isomería espacial. Es importante entender que las transformaciones cis y alquenos son posibles solo para la posición del doble enlace 2 y 3.
Cuando los radicales de hidrocarburos están en el mismo plano, se forma cis, midiendo el hexeno-2, y cuando los radicales están ubicados en diferentes planos, la forma trans del hexeno es 2.
Isómeros entre clases C6H12
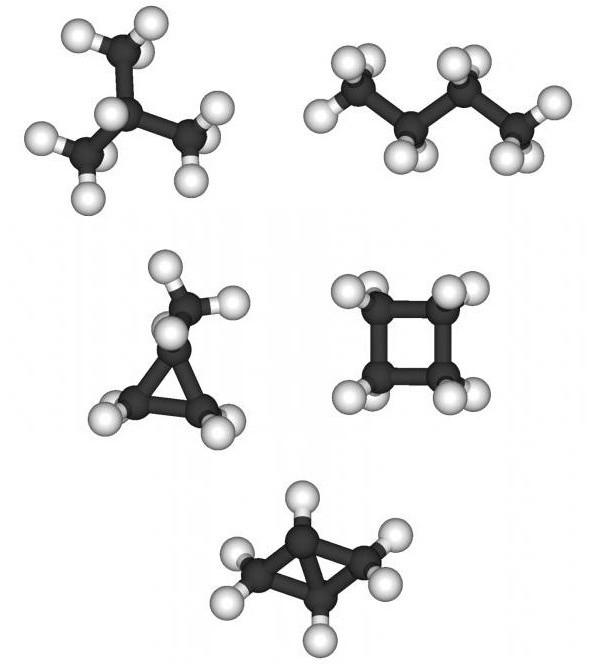
Discutir cómo componer isómeros yhomólogos, no debemos olvidarnos de una variante como la isomería interclase. Para los hidrocarburos insaturados de la serie del etileno que tienen la fórmula general CnH2n, tales isómeros son cicloalcanos. Una característica de esta clase de hidrocarburos es la presencia de una estructura cíclica (cerrada) con enlaces simples saturados entre átomos de carbono. Pueden elaborarse fórmulas para ciclohexano, metilciclopentano, dimetilciclobutano, trimetilciclopropano.
Conclusión
La química orgánica es multifacética y misteriosa.La cantidad de materia orgánica es cientos de veces mayor que la cantidad de compuestos inorgánicos. Este hecho se explica fácilmente por la existencia de un fenómeno tan singular como la isomería. Si en la misma serie homóloga hay sustancias similares en propiedades y estructura, entonces cuando cambia la posición de los átomos de carbono en la cadena, aparecen nuevos compuestos, llamados isómeros. Solo después de la aparición de la teoría de la estructura química de las sustancias orgánicas fue posible clasificar todos los hidrocarburos para comprender los detalles de cada clase. Una de las disposiciones de esta teoría se refiere directamente al fenómeno de la isomería. El gran químico ruso pudo comprender, explicar y probar que las propiedades químicas de una sustancia, su actividad de reacción y su aplicación práctica dependen de la disposición de los átomos de carbono. Al comparar el número de isómeros formados por alcanos saturados y alquenos insaturados, los alquenos están indudablemente a la cabeza. Esto se explica por el hecho de que hay un doble enlace en sus moléculas. Es lo que permite a esta clase de sustancias orgánicas formar no solo alquenos de diferentes tipos y estructuras, sino también hablar de isomería de mi clase con cicloalcanos.





