Wenn zwei oder mehr Atome in die Chemikalie eintretenBindungen miteinander, Moleküle entstehen. Es spielt keine Rolle, ob diese Atome gleich sind oder ob sie sich in Form und Größe völlig voneinander unterscheiden. Wir werden herausfinden, wie groß die Moleküle sind und wovon sie abhängen.

Was sind Moleküle?
Seit Jahrtausenden spekulieren Wissenschaftler darüberdas Geheimnis des Lebens, darüber, was genau zu Beginn passiert. Nach den ältesten Kulturen besteht das Leben und alles - alles auf dieser Welt aus den Grundelementen der Natur - Erde, Luft, Wind, Wasser und Feuer. Im Laufe der Zeit begannen jedoch viele Philosophen, die Idee zu vertreten, dass alle Dinge aus winzigen, unteilbaren Dingen bestehen, die nicht geschaffen und zerstört werden können.
Allerdings erst nach dem Erscheinen der Atomtheorie undIn der modernen Chemie begannen Wissenschaftler zu postulieren, dass Teilchen zusammengenommen die Grundbausteine aller Dinge hervorbrachten. So entstand der Begriff, der sich im Kontext der modernen Partikeltheorie auf die kleinsten Masseneinheiten bezieht.
Nach seiner klassischen Definition ist ein MolekülEs ist das kleinste Partikel einer Substanz, das zur Aufrechterhaltung seiner chemischen und physikalischen Eigenschaften beiträgt. Es besteht aus zwei oder mehr Atomen sowie Gruppen derselben oder verschiedener Atome, die durch chemische Kräfte zusammengehalten werden.
Wie groß sind die Moleküle? In der 5. Klasse gibt die Naturgeschichte (ein Schulfach) nur eine allgemeine Vorstellung von Größe und Form. Im Detail wird dieses Thema in der High School im Chemieunterricht untersucht.
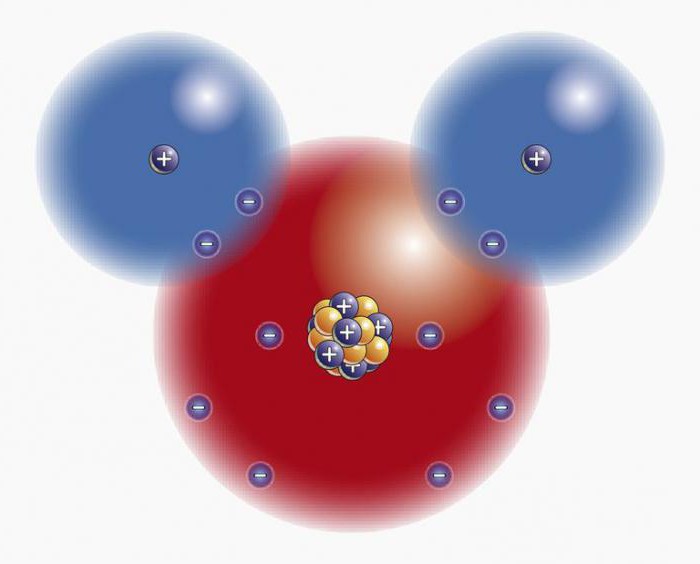
Beispiele für Moleküle
Moleküle können einfach oder komplex sein. Hier sind einige Beispiele:
- X2O (Wasser);
- H2 (Stickstoff);
- Oh!3 (Ozon);
- CaO (Calciumoxid);
- C6X12Oh!6 (Glucose).
Moleküle, die aus zwei oder mehr Elementen bestehenwerden Verbindungen genannt. Wasser, Calciumoxid und Glucose sind also Bestandteile. Nicht alle Verbindungen sind Moleküle, aber alle Moleküle sind Verbindungen. Wie groß können sie sein? Wie groß ist das Molekül? Es ist eine bekannte Tatsache, dass fast alles um uns herum aus Atomen besteht (außer Licht und Ton). Ihr Gesamtgewicht ist die Masse des Moleküls.

Molekulare Masse
Wenn es um die Größe von Molekülen geht, gehen die meisten Wissenschaftler vom Molekulargewicht aus. Dies ist das Gesamtgewicht aller darin enthaltenen Atome:
- Wasser, bestehend aus zwei Wasserstoffatomen (jeweils mit einer Atommasseneinheit) und einem Sauerstoffatom (16 Atommasseneinheiten), hat ein Molekulargewicht von 18 (genauer gesagt 18.01528).
- Glucose hat ein Molekulargewicht von 180.
- Sehr lange DNA kann ein Molekulargewicht von etwa 1010 haben (das ungefähre Gewicht eines menschlichen Chromosoms).

Messung in Nanometern
Neben der Masse können wir auch messen,Wie groß sind die Moleküle in Nanometern? Die Wassereinheit hat einen Durchmesser von etwa 0,27 Nm. DNA erreicht einen Durchmesser von 2 nm und kann sich bis zu mehreren Metern Länge erstrecken. Es ist schwer vorstellbar, wie solche Abmessungen in einen Käfig passen. Das Verhältnis von Länge zu Dicke der DNA ist erstaunlich. Es ist 1 / 100.000.000, wie ein menschliches Haar die Länge eines Fußballfeldes.

Formen und Größen
Wie groß sind die Moleküle?Sie kommen in allen Formen und Größen. Wasser und Kohlendioxid gehören zu den kleinsten, Proteine zu den größten. Moleküle sind Elemente, die aus Atomen bestehen, die aneinander gebunden sind. Das Verständnis des Aussehens von Molekülen ist traditionell Teil der Chemie. Neben ihrem unverständlich seltsamen chemischen Verhalten ist eine der wichtigsten Eigenschaften von Molekülen ihre Größe.
Wo kann es besonders hilfreich sein zu wissenWie groß sind die Moleküle? Die Beantwortung dieser und vieler weiterer Fragen hilft im Bereich der Nanotechnologie, da sich das Konzept von Nanorobotern und intelligenten Materialien zwangsläufig mit den Auswirkungen von Molekülgrößen und -formen beschäftigt.

Wie groß sind die Moleküle?
In Klasse 5 gibt Naturgeschichte zu diesem Themanur allgemeine Information, dass alle Moleküle aus Atomen bestehen, die sich in ständiger ungeordneter Bewegung befinden. Schon in der High School sieht man in Chemielehrbüchern Strukturformeln, die der tatsächlichen Form von Molekülen ähneln. Es ist jedoch unmöglich, ihre Länge mit einem normalen Lineal zu messen, und dazu müssen Sie wissen, dass Moleküle dreidimensionale Objekte sind. Ihr Bild auf Papier ist eine Projektion auf eine zweidimensionale Ebene. Die Länge eines Moleküls ändert sich durch die Bindungslängen seiner Winkel. Es gibt drei Hauptpunkte:
- Der Tetraederwinkel beträgt 109 °, wenn alle Bindungen dieses Atoms mit allen anderen Atomen einfach sind (nur ein Strich).
- Der Winkel des Sechsecks beträgt 120°, wenn ein Atom eine Doppelbindung mit einem anderen Atom hat.
- Der Linienwinkel beträgt 180°, wenn ein Atom entweder zwei Doppelbindungen oder eine Dreifachbindung mit einem anderen Atom hat.
Reale Winkel weichen oft von diesen Winkeln ab, da eine Vielzahl unterschiedlicher Effekte berücksichtigt werden müssen, einschließlich elektrostatischer Wechselwirkungen.
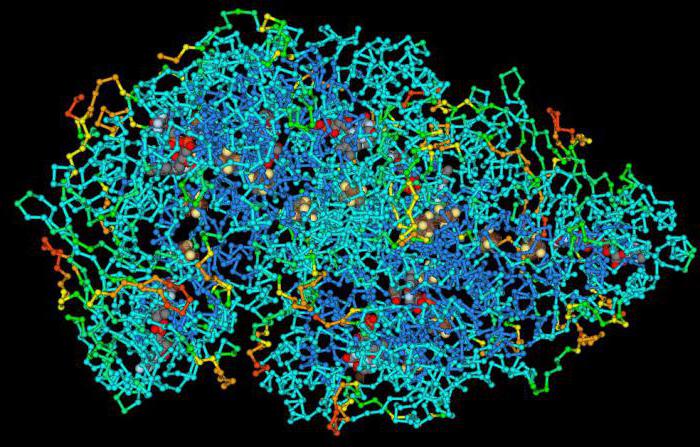
Wie man sich die Größe von Molekülen vorstellt: Beispiele
Wie groß sind die Moleküle?In der 5. Klasse sind die Antworten auf diese Frage, wie bereits gesagt, allgemeiner Natur. Die Schüler wissen, dass die Größe der genannten Gelenke sehr klein ist. Wenn Sie beispielsweise ein Sandmolekül in einem einzigen Sandkorn in ein ganzes Sandkorn verwandeln, können Sie unter der resultierenden Masse ein Haus mit fünf Etagen verstecken. Wie groß sind die Moleküle? Die kurze Antwort, die auch wissenschaftlicher ist, lautet wie folgt.
Molekulargewicht entspricht dem Verhältnisdie Masse der gesamten Substanz zur Anzahl der Moleküle in der Substanz oder das Verhältnis von Molmasse zur Avogadro-Konstante. Die Maßeinheit ist das Kilogramm. Das durchschnittliche Molekulargewicht beträgt 10-23-10-26 kg. Nehmen Sie zum Beispiel Wasser. Sein Molekulargewicht beträgt 3 x 10 -26 kg

Wie beeinflusst die Größe eines Moleküls die Anziehungskräfte?
Verantwortlich für die Anziehung zwischen Molekülenist die elektromagnetische Kraft, die sich durch Anziehung gegensätzlicher und Abstoßung ähnlicher Ladungen manifestiert. Die elektrostatische Kraft, die zwischen entgegengesetzten Ladungen existiert, dominiert die Wechselwirkungen zwischen Atomen und zwischen Molekülen. Die Gravitationskraft ist in diesem Fall so klein, dass sie vernachlässigt werden kann.
In diesem Fall beeinflusst die Größe des Moleküls die StärkeAnziehung durch die Elektronenwolke zufälliger Verzerrungen, die sich aus der Verteilung der Elektronen des Moleküls ergeben. Bei unpolaren Partikeln, die nur schwache Van-der-Waals-Wechselwirkungen oder Dispersionskräfte aufweisen, hat die Größe der Moleküle einen direkten Einfluss auf die Größe der Elektronenwolke, die das angegebene Molekül umgibt. Je größer es ist, desto größer ist das geladene Feld, das es umgibt.
Eine größere Elektronenwolke bedeutet, dass zwischenEs können mehr elektronische Wechselwirkungen mit benachbarten Molekülen auftreten. Dadurch entwickelt ein Teil des Moleküls vorübergehend eine positive Teilladung, während der andere eine negative Teilladung entwickelt. Dabei kann das Molekül die Elektronenwolke der Nachbarwolke polarisieren. Anziehung tritt auf, weil eine teilweise positive Seite eines Moleküls von einer teilweise negativen Seite eines anderen angezogen wird.

Fazit
Welche Größe haben die Moleküle also?In der Naturwissenschaft findet man, wie wir herausgefunden haben, nur eine bildliche Vorstellung von der Masse und Größe dieser kleinsten Teilchen. Aber wir wissen, dass es einfache und komplexe Zusammenhänge gibt. Und die zweite beinhaltet so etwas wie ein Makromolekül. Es ist eine sehr große Einheit, wie beispielsweise ein Protein, das normalerweise durch Polymerisieren kleinerer Untereinheiten (Monomere) hergestellt wird. Sie haben normalerweise Tausende von Atomen oder mehr.
Die häufigsten Makromoleküle inBiochemie sind Biopolymere (Nukleinsäuren, Proteine, Kohlenhydrate und Polyphenole) und große nicht-polymere Moleküle (wie Lipide). Synthetische Makromoleküle umfassen gängige Kunststoffe und synthetische Fasern sowie experimentelle Materialien wie Kohlenstoff-Nanoröhrchen.





