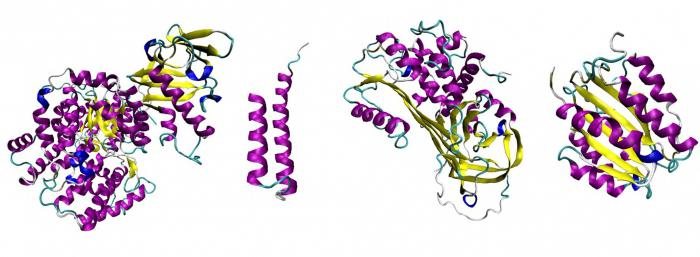
Het menselijk lichaam wordt biochemisch genoemdde fabriek is niet voor niets. Inderdaad vinden er elke minuut duizenden, tienduizenden en honderdduizenden processen van oxidatie, splitsing, reductie en andere reacties in plaats. Wat zorgt ervoor dat ze met zo'n enorme snelheid kunnen stromen en elke cel van energie, voeding en zuurstof voorzien?
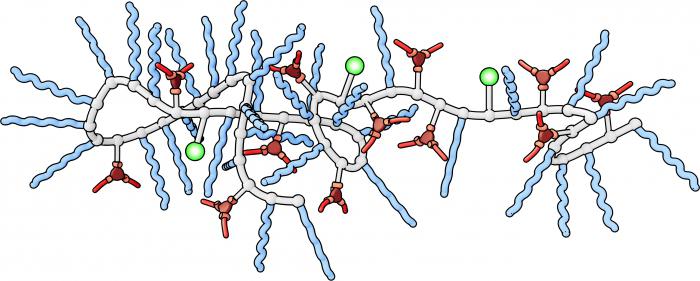
Katalysatoren begrijpen
In zowel anorganische als organische chemiezeer veel gebruikt zijn speciale stoffen die het verloop van chemische reacties met enkele duizenden en soms zelfs miljoenen keren kunnen versnellen. De namen van deze verbindingen zijn "katalysatoren". In anorganische chemie zijn dit metaaloxiden, platina, zilver, nikkel en andere.
Hun belangrijkste actie is de vorming van tijdelijkcomplexen met de reactiedeelnemers, vanwege een afname van de activeringsenergie, wordt het proces verschillende keren sneller uitgevoerd. Daarna valt het complex uiteen en kan de katalysator uit de bol worden verwijderd in dezelfde kwantitatieve en kwalitatieve samenstelling als vóór het begin van het proces.
Er zijn twee opties voor katalytische reacties:
- homogeen - versneller en deelnemers in dezelfde aggregatietoestand;
- heterogeen - versneller en deelnemers in verschillende staten, er is een fasegrens.
Daarnaast zijn er ook tegengestelde in actie.verbindingen - remmers. Ze zijn gericht op het vertragen van de benodigde reacties. Ze verminderen bijvoorbeeld de hoeveelheid tijd die nodig is om corrosie te vormen.
Biologische katalysatoren zijn inherent verschillend van anorganische katalysatoren en hun eigenschappen zijn enigszins specifiek. Daarom is katalyse in levende systemen anders.
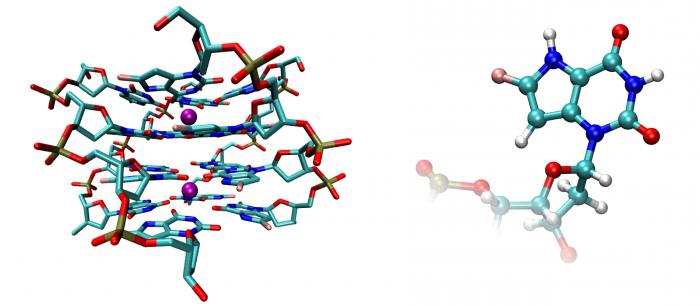
Enzymen - wat zijn dat?
Het is bewezen dat als de actie van bijzonder isstoffen die de aangegeven processen versnellen, werden niet in levende systemen uitgevoerd, dan zou een gewone appel in de maag ongeveer twee dagen worden verteerd. Gedurende zo'n tijd zouden ontbindingsprocessen en bedwelming met vervalproducten beginnen. Dit gebeurt echter niet en het fruit is in anderhalf uur volledig verwerkt. Dit wordt bereikt door biologische katalysatoren, die in grote hoeveelheden in de samenstelling van elk organisme aanwezig zijn. Maar wat zijn ze en waarop is zo'n actie gebaseerd?
Biologische katalysatoren van eiwitachtige aard zijnenzymen. Ze zijn gebaseerd op een complexe structurele organisatie met een aantal specifieke eigenschappen. Simpel gezegd, dit zijn unieke eiwitten die in staat zijn om de activeringsenergie van processen in levende organismen te verminderen en deze uit te voeren met een snelheid die de gebruikelijke waarden miljoenen keren overschrijdt.
Er zijn veel voorbeelden van dergelijke moleculen:
- catalase;
- amylase;
- oxyreductase;
- glucose oxidase;
- lipase;
- invertase;
- lysozym;
- protease en anderen.
We kunnen dus concluderen:enzymen zijn biologische katalysatoren van eiwitachtige aard die als krachtige versnellers werken, waardoor duizenden processen in levende organismen met een zeer hoge snelheid kunnen worden uitgevoerd. Spijsvertering, oxidatie en reductie zijn gebaseerd op hun werking.
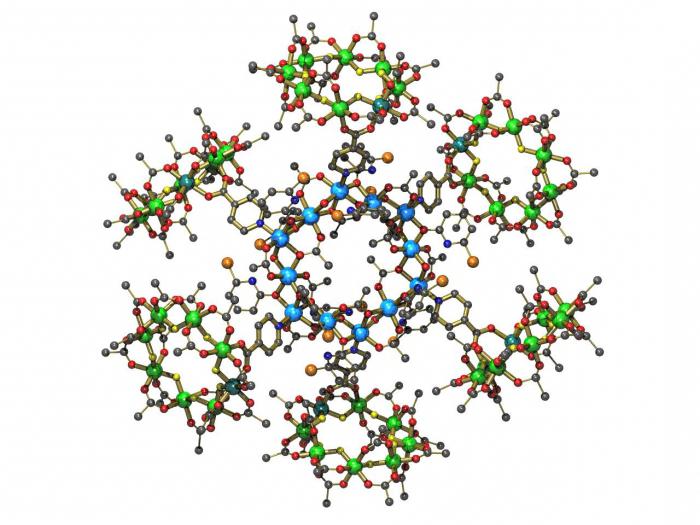
Overeenkomsten tussen anorganische en eiwitkatalysatoren
Enzymen als biologische katalysatoren hebben een aantal eigenschappen die vergelijkbaar zijn met die van anorganische. Deze omvatten het volgende:
- Alleen thermodynamisch mogelijke reacties worden versneld.
- Ze hebben geen invloed op de verschuiving van chemisch evenwicht in evenwichtssystemen, maar versnellen evenzeer zowel directe als omgekeerde processen.
- Daardoor blijven alleen de producten in de sfeer van de reactie; de katalysator zit er niet bij.
Naast de gelijkenis zijn er echter ook onderscheidende kenmerken van enzymen.
Verschillen van nature
Biologische katalysatoren hebben verschillende specifieke kenmerken:
- Hoge mate van selectiviteit. Dat wil zeggen, één eiwit kan alleen een specifieke reactie of een groep van vergelijkbare reacties activeren. Meestal werkt het schema "enzym - substraat van één proces".
- Een extreem hoge activiteit, omdat sommige soorten eiwitten reacties miljoenen keren kunnen versnellen.
- Enzymen zijn sterk afhankelijk van omgevingsomstandigheden.Ze vertonen alleen activiteit in een bepaald temperatuurbereik. Ook de pH van de omgeving wordt sterk beïnvloed. Er is een curve die de waarden van het minimum, maximum en optimum toont in termen van indicatoren voor elk enzym.
- Er zijn speciale verbindingen die effectoren worden genoemd en die de aard van biologische katalysatoren kunnen remmen of, omgekeerd, positief kunnen beïnvloeden.
- Het substraat waarop het enzym werkt, moetwees strikt specifiek. Er is een theorie die een sleutel en een slot wordt genoemd. Het beschrijft het werkingsmechanisme van het enzym op het substraat. De katalysator wordt als een sleutel door zijn actieve centrum in het substraat opgenomen en de reactie begint.
- Na het proces wordt het enzym gedeeltelijk of volledig vernietigd.
Het is dus duidelijk dat het belang van eiwitkatalysatoren buitengewoon hoog is voor levende organismen. Hun optreden is echter onderworpen aan bepaalde regels en wordt beperkt door het kader van milieuvoorwaarden.

Katalyse studeren op school
Als onderdeel van het schoolcurriculum, katalysatorengestudeerd in zowel chemie als biologie. In scheikundelessen worden ze bestudeerd vanuit het oogpunt van stoffen waarmee industriële syntheses kunnen worden uitgevoerd, om een groot aantal verschillende producten te verkrijgen. Bij biologielessen wordt gekeken naar biologische katalysatoren. Graad 9 omvat de studie van moleculaire biologie en de basis van biochemie. Daarom ontvangen studenten in deze fase van het onderwijs de basiskennis van enzymen als actieve stoffen in de organismen van levende wezens.
In de klas worden experimenten uitgevoerd die de chemische activiteit van deze stoffen bij bepaalde temperatuurbereiken en de pH van de omgeving bevestigen:
- onderzoek naar het effect van waterstofperoxide als katalysator op rauwe en gekookte wortelen;
- impact op vlees (thermisch verwerkt en rauw), aardappelen en andere producten.
Enzymen in het menselijk lichaam
Iedere student, voldoende opgeleid ende lijn van het middelbaar onderwijs gepasseerd, weet wat biologische katalysatoren worden genoemd. Enzymen in het lichaam hebben een strikt specifieke specialisatie. Daarom kunt u voor elk proces uw eigen katalytische stof een naam geven.

Alle enzymen in het lichaam kunnen dus in verschillende groepen worden verdeeld:
- oxidoreductases zoals catalase of alcohol dehydrogenase;
- transferase - kenase;
- hydrolasen die belangrijk zijn voor de spijsvertering: pepsine, amylase, lipoproteïnelipase, esterase en andere;
- ligasen, zoals DNA-polymerase;
- isomerase;
- lyasen.
Omdat al deze verbindingen eiwitten bevattenaard, evenals het complex van vitamines in de samenstelling, dan is een toename van de lichaamstemperatuur beladen met denaturatie van de structuur en daarom het stoppen van alle biochemische reacties. In dit geval is het lichaam bijna dood. Daarom moet de hoge lichaamstemperatuur tijdens ziekte worden verlaagd.
Industrieel gebruik van proteïnekatalysatoren
Enzymen worden vaak gebruikt in verschillende industrieën:
- chemisch;
- textiel;
- eten.
In de winkelrekken zie je wasmiddelen en waspoeders die enzymen bevatten - dit zijn enzymen die de kwaliteit van het wassen van kleding verbeteren.

Waar zijn biologische katalysatoren voor?
Het belang ervan is moeilijk te overschatten.Ze laten immers niet alleen levende organismen toe om te leven, ademen, eten, metabolische processen uit te voeren, maar geven ons ook de mogelijkheid om industrieel afval te vernietigen, medicijnen te ontvangen, hun gezondheid en de toestand van het milieu te beschermen en te behouden.