Alle studerende står i fysikundervisning medet sådant koncept som "specifik varme". I de fleste tilfælde glemmer folk skoledefinitionen og forstår ofte slet ikke betydningen af dette udtryk. På tekniske universiteter vil størstedelen af studerende før eller senere stå over for den specifikke varmekapacitet. Måske inden for rammerne af fysikstudiet, eller måske vil nogen have en sådan disciplin som "varmekonstruktion" eller "teknisk termodynamik". I dette tilfælde bliver du nødt til at huske skolens læseplan. Så definitionen, eksempler, betydninger for nogle stoffer betragtes nedenfor.
definition
Specifik varme er fysisken mængde, der karakteriserer, hvor meget varme der skal tilføres en enhed af stof eller fjernes fra en enhed, for at dens temperatur kan ændre sig med en grad. Det er vigtigt at annullere, hvilket ikke betyder noget, grader Celsius, Kelvin og Fahrenheit, det vigtigste er temperaturændringen med en.
Specifik varme har sin egen enhedmålinger - i det internationale enhedssystem (SI) - Joule divideret med produktet af kilo og Kelvin-grad, J / (kg · K); off-system enhed er forholdet mellem kalorie og produkt af kilo og grad Celsius, cal / (kg · ° C). Denne værdi er oftest betegnet med bogstavet c eller C, nogle gange bruges indekser. For eksempel, hvis trykket er konstant, så er indekset p, og hvis lydstyrken er konstant, så v.
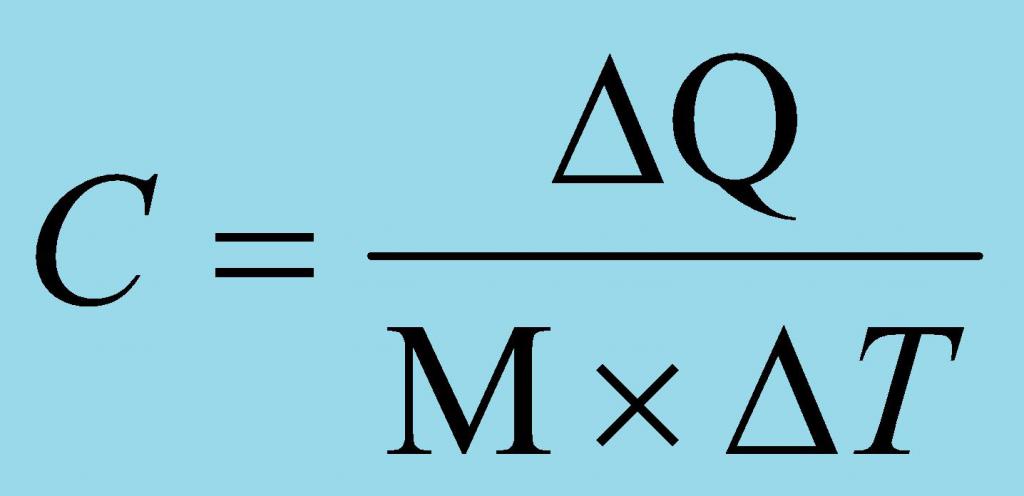
Definition variationer
Flere definitioner er muligeaf den diskuterede fysiske mængde. Ud over ovenstående betragtes definitionen som acceptabel, som siger, at den specifikke varme er forholdet mellem et stofs varmekapacitet og dets masse. I dette tilfælde er det nødvendigt at forstå, hvad "varmekapacitet" er. Så varmekapacitet kaldes en fysisk størrelse, der viser, hvor meget varme der skal tilføres et legeme (stof) eller fjernes for at ændre værdien af dets temperatur med en. Den specifikke varmekapacitet for et stofs masse større end et kilogram bestemmes på samme måde som for en enkelt værdi.
Nogle eksempler og betydninger for forskellige stoffer

Det er eksperimentelt fundet, at for forskellige stofferdenne betydning er anderledes. For eksempel er vandets specifikke varmekapacitet 4,187 kJ / (kg · K). Den største værdi af denne fysiske mængde for brint er 14.300 kJ / (kg K), den mindste for guld er 0,129 kJ / (kg K). Hvis du har brug for en værdi for et bestemt stof, skal du tage en referencebog og finde de tilsvarende tabeller og i dem - værdierne af interesse. Imidlertid gør moderne teknologier det muligt at fremskynde søgningsprocessen til tider - det er nok på enhver telefon, der har mulighed for at gå ind på World Wide Web, skriv spørgsmålet om interesse i søgefeltet, start søgningen og søg efter svar baseret på resultaterne. I de fleste tilfælde skal du følge det første link. Men nogle gange behøver du slet ikke gå nogen andre steder - i den korte beskrivelse af oplysningerne kan du se svaret på spørgsmålet.

De mest almindelige stoffer, for hvilke der søges varmekapacitet, herunder specifik varmekapacitet, er:
- luft (tør) - 1,005 kJ / (kg K),
- aluminium - 0,930 kJ / (kg K),
- kobber - 0,385 kJ / (kg K),
- ethanol - 2.460 kJ / (kg K),
- jern - 0,444 kJ / (kg K),
- kviksølv - 0,139 kJ / (kg K),
- ilt - 0,920 kJ / (kg K),
- træ - 1.700 kJ / (kg K),
- sand - 0,835 kJ / (kg K).












