Begivenhederne i den fysiske verden er uløseligt forbundet medændringer i temperatur. Hver person lærer hende at kende i den tidlige barndom, når han indser, at isen er kold, og kogende vand brænder. Samtidig kommer forståelsen af, at temperaturændringsprocesserne ikke sker øjeblikkeligt. Senere, i skolen, lærer eleven, hvad der er forbundet med varmebevægelse. Og de processer, der er forbundet med temperatur, er en hel sektion af fysik tildelt.

Hvad er temperatur?
Dette videnskabelige koncept blev introduceret for at erstatte det almindeligevilkår. Ord som varmt, koldt eller varmt optræder konstant i hverdagen. De taler alle om graden af kropsvarme. Sådan defineres det i fysikken, kun med den tilføjelse, at det er en skalær størrelse. Temperaturen har jo ingen retning, men kun en numerisk værdi.
I det internationale system af enheder (SI), temperaturmålt i grader Celsius (ºС). Men i mange formler, der beskriver termiske fænomener, er det nødvendigt at oversætte det til Kelvin (K). Til dette er der en simpel formel: T = t + 273. I den er T temperaturen i Kelvin, og t er i Celsius. Kelvin-skalaen er forbundet med begrebet absolutte nultemperaturer.
Der er flere temperaturskalaer.I Europa og Amerika bruges f.eks. Fahrenheit (F). Derfor skal de kunne skrive dem ned i Celsius. For at gøre dette er det nødvendigt at trække 32 fra aflæsningerne i F og derefter dividere det med 1,8.

Hjemmeeksperiment
I sin forklaring er det nødvendigt at kende sådanne begreber som temperatur, termisk bevægelse. Og det er nemt at udføre dette eksperiment.
For ham skal du tage tre beholdere.De skal være store nok til at passe dine hænder nemt. Fyld dem med vand af forskellige temperaturer. I den første skal det være meget koldt. I den anden - varmet op. Hæld varmt vand i den tredje, hvor det vil være muligt at holde en hånd.
Nu selve oplevelsen. Dyp din venstre hånd i en beholder med koldt vand, og din højre hånd med den varmeste. Vent et par minutter. Tag dem ud og nedsænk dem straks i en beholder med varmt vand.
Resultatet vil være uventet.Den venstre hånd vil føle, at vandet er varmt, den højre vil føle fornemmelsen af koldt vand. Dette skyldes det faktum, at termisk ligevægt først etableres med de væsker, som hænderne først er nedsænket i. Og så er denne balance drastisk forstyrret.
Grundlæggende principper for molekylær kinetisk teori
Den beskriver alle termiske fænomener. Og disse udsagn er ret enkle. Derfor, når man taler om termisk bevægelse, skal disse bestemmelser kendes.
Først:stoffer dannes af de mindste partikler, der ligger i nogen afstand fra hinanden. Desuden kan disse partikler være både molekyler og atomer. Og afstanden mellem dem er mange gange større end partikelstørrelsen.
For det andet: i alle stoffer er der en termisk bevægelse af molekyler, som aldrig stopper. I dette tilfælde bevæger partiklerne sig tilfældigt (kaotisk).
For det tredje: partiklerne interagerer med hinanden. Denne handling skyldes kræfterne til tiltrækning og frastødning. Deres værdi afhænger af afstanden mellem partiklerne.
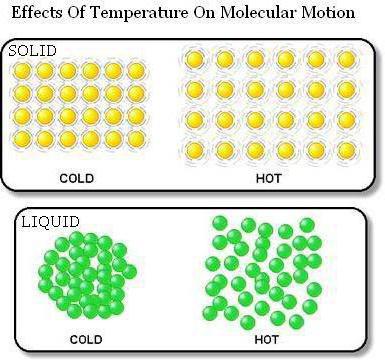
Bekræftelse af den første bestemmelse i ICB
Bevis på, at legemer er lavet af partiklermellem hvilke der er huller, tjener deres termiske ekspansion. Så når kroppen opvarmes, øges dens størrelse. Dette sker på grund af fjernelse af partikler fra hinanden.
En anden bekræftelse af ovenstående erdiffusion. Det vil sige penetration af molekyler af et stof mellem partiklerne i et andet. Desuden viser denne bevægelse sig at være gensidig. Diffusion skrider frem, jo hurtigere jo længere molekylerne er fra hinanden. Derfor vil gensidig penetration i gasser ske meget hurtigere end i væsker. Og i faste stoffer tager diffusion år.
Sidstnævnte proces forklarer i øvrigt også den termiske bevægelse. Når alt kommer til alt, sker den gensidige indtrængning af stoffer i hinanden uden nogen indblanding udefra. Men det kan accelereres ved at opvarme kroppen.
Bekræftelse af den anden bestemmelse i ICB
Et klart bevis på, at der ertermisk bevægelse er den brownske bevægelse af partikler. Det overvejes for suspenderede partikler, det vil sige for dem, der er væsentligt større end stoffets molekyler. Disse partikler kan være pletter af støv eller korn. Og de skal placeres i vand eller gas.
Årsagen til den vægtedes uberegnelige bevægelsepartikler i, at molekyler virker på det fra alle sider. Deres handling er uberegnelig. Størrelsen af påvirkningerne på hvert tidspunkt er forskellig. Derfor er den resulterende kraft rettet den ene eller den anden vej.
Hvis vi taler om hastigheden af termisk bevægelse af molekyler, så er der et specielt navn for det - den gennemsnitlige kvadratiske rod. Det kan beregnes ved hjælp af formlen:
v = √ [(3kT)/m0].
I den er T temperaturen i Kelvin, m0 Er massen af et molekyle, k er Boltzmann-konstanten (k = 1,38 * 10-23 J/K).

Bekræftelse af den tredje bestemmelse i ICB
Partikler tiltrækker og frastøder. Ved at forklare mange af de processer, der er forbundet med termisk bevægelse, viser denne viden sig at være vigtig.
Når alt kommer til alt, afhænger vekselvirkningens kræfter af aggregatetmateriens tilstand. Så gasser har dem praktisk talt ikke, da partiklerne fjernes så meget, at deres virkning ikke manifesteres. I væsker og faste stoffer er de mærkbare og sikrer bevarelsen af stoffets volumen. I sidstnævnte garanterer de også at holde sig i form.
Bevis på eksistensen af tiltrækningskræfterne ogfrastødning er udseendet af elastiske kræfter under deformation af kroppe. Så med forlængelse øges tiltrækningskræfterne mellem molekyler, og med kompression frastødning. Men i begge tilfælde bringer de kroppen tilbage til sin oprindelige form.

Gennemsnitlig energi af termisk bevægelse
Det kan skrives ud fra den grundlæggende ligning for MKT:
(pV)/N = (2E)/3.
I denne formel er p trykket, V er volumenet, N er antallet af molekyler, og E er den gennemsnitlige kinetiske energi.
På den anden side kan denne ligning skrives sådan:
(pV)/N = kT.
Hvis du kombinerer dem, får du følgende lighed:
(2E) / 3 = kT.
Af den følger følgende formel for den gennemsnitlige kinetiske energi af molekyler:
E = (3kT) / 2.
Heraf kan det ses, at energien er proportional medstoffets temperatur. Det vil sige, at når sidstnævnte stiger, bevæger partiklerne sig hurtigere. Dette er essensen af termisk bevægelse, som eksisterer, så længe der er en anden temperatur end det absolutte nulpunkt.








