دعونا نتحدث عن كيفية العثور على البروتونات والنيوترونات والإلكترونات. في ذرة هناك ثلاثة أنواع من الجسيمات الأولية ، لكل منها شحنتها الابتدائية الخاصة ، الكتلة.

هيكل النواة
من أجل فهم كيفية العثور على البروتونات ،النيوترونات والالكترونات ، فإننا سوف نمثل ملامح بنية النواة. هذا هو الجزء الرئيسي من الذرة. داخل النواة توجد البروتونات والنيوترونات ، وتسمى النيوكليونات. داخل الجوهر ، يمكن لهذه الجسيمات عبور بعضها البعض.
على سبيل المثال ، لإيجاد البروتونات والنيوترونات ، والإلكترونات في ذرة الهيدروجين ، من الضروري معرفة رقمها الترتيبي. إذا أخذنا في الاعتبار أن هذا العنصر هو رأس النظام الدوري ، فإن نواته تحتوي على بروتون واحد.
يبلغ قطر النواة الذرية عشرة ألاف من الحجم الكلي للذرة. في ذلك يتركز الجزء الأكبر من الذرة بأكملها. بالكتلة ، تتجاوز النواة بمقدار ألف مرة مجموع كل الإلكترونات الموجودة في الذرة.
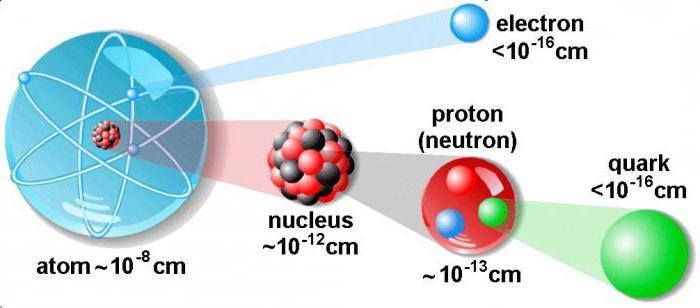
خصائص الجسيمات
فكِّر في كيفية العثور على بروتونات ونيوترونات والإلكترونات في الذرة ، ونحن نتعرف على ميزاتها. البروتون هو جسيم أولي يتطابق مع نواة ذرة الهيدروجين. كتلته تتجاوز الإلكترون في 1836 مرة. يتم استخدام شحنة كهربائية لتحديد وحدة الكهرباء التي تمر عبر موصل مع مقطع عرضي معين.
كل ذرة في النواة لها عدد معين من البروتونات. إنها قيمة ثابتة ، تميز الخصائص الكيميائية والفيزيائية لعنصر معين.
كيفية العثور على البروتونات والنيوترونات والإلكترونات في الذرةالكربون؟ الرقم الترتيبي لهذا العنصر الكيميائي هو 6 ، لذلك ، تحتوي النواة على ستة بروتونات. ووفقًا للنموذج الكوكبي لهيكل الذرة ، تتحرك ستة إلكترونات حول النواة على طول المدارات. لتحديد عدد النيوترونات من قيمة الكتلة الذرية النسبية للكربون (12) ، اطرح عدد البروتونات (6) ، مما أسفر عن ستة نيوترونات.
بالنسبة إلى ذرة الحديد ، فإن عدد البروتونات يناظر 26 ، أي أن هذا العنصر يحتوي على رقم ترتيبي رقم 26 في الجدول الدوري.
النيوترون محايدة كهربيًاجسيم غير مستقر في الحالة الحرة. إن النيوترون قادر على التحول التلقائي إلى بروتون مشحون بإيجابية ، ينبعث منه مضادات antineutrinos والإلكترونات. متوسط عمر النصف هو 12 دقيقة. الرقم الشامل هو القيمة الإجمالية لعدد البروتونات والنيوترونات داخل نواة الذرة. دعونا نحاول معرفة كيفية العثور على بروتونات ونيوترونات وإلكترونات في الأيون؟ إذا اكتشفت الذرة حالة أكسدة إيجابية أثناء تفاعل كيميائي مع عنصر آخر ، فإن عدد البروتونات والنيوترونات لا يتغير فيه ، فإن الإلكترونات فقط تصبح أقل.

استنتاج
كانت هناك العديد من النظريات المتعلقةهيكل الذرة ، ولكن أيا منها لم يكن قابلا للتطبيق. حتى الإصدار الذي أنشأه رذرفورد ، لم يكن هناك تفسير مفصل للموقع داخل نواة البروتونات والنيوترونات ، وكذلك الدوران في مدارات الإلكترونات الدائرية. بعد ظهور نظرية البنية الكوكبية للذرة ، فإن الباحثين لديهم الفرصة ليس فقط لتحديد عدد الجسيمات الأولية في الذرة ، ولكن أيضا للتنبؤ بالخصائص الفيزيائية والكيميائية لعنصر كيميائي معين.











