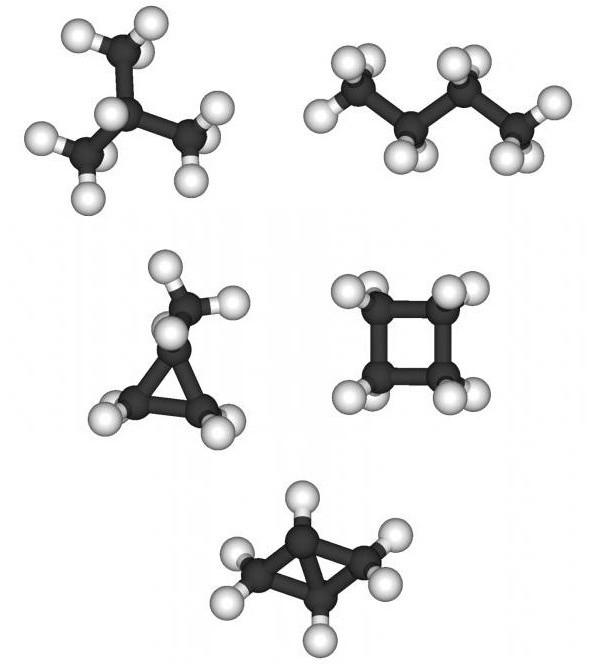
Hydrokarboner er den enkleste klassen av organiskestoffer, har molekylene deres atomer med bare to kjemiske grunnstoffer - karbon og hydrogen. De fleste klasser av organiske forbindelser erholdes fra forskjellige hydrokarboner ved bruk av kjemiske syntesemetoder.
Hydrokarboner er delt inn i to underklasser -acyklisk og syklisk. Følgende grupper tilhører acykliske hydrokarboner eller fete hydrokarboner eller alifatiske hydrokarboner: mettede hydrokarboner (alkaner), umettede (alkener, alkyner, diener), acykliske terpener. Sykliske hydrokarboner er representert av cykloparaffingrupper, arenaer og sykliske terpener. Noen ganger klassifiseres terpener som gjenstander for studier i bioorganisk kjemi.
Mettede hydrokarboner (alkaner) - forbindelserkarbon og hydrogen, i hvilke molekylene alle valensene som er igjen etter at karbonatomer er koblet til hverandre ved en enkel binding, er mettet med hydrogenatomer. Alle alkaner kan betraktes som derivater eller homologer av metan. Hvis ett hydrogenatom trekkes fra metan, som har molekylformelen CH4, dannes en partikkel - CH3-radikalen. På grunn av det faktum at olerod vanligvis er tetravalent i et organisk stoffmolekyl, forårsaker kombinasjonen av to slike radikaler utseendet til den andre representanten for den homologe serien - etan (C2H6). Hvis ett hydrogenatom trekkes fra etan, dannes et etylradikal som, etter kombinasjon med CH3, danner en tredje homolog, propan.
Ved å analysere strukturformelen til propan er det lett åfor å fastslå at molekylet inneholder to typer karbonatomer - primære og sekundære. Hvert primære karbonatom er bundet til ett karbonatom av en av valensene, og det sekundære - av to valenser med to karbonatomer. Hvis du trekker fra hydrogenatomet fra det primære karbonatomet i propan, dannes primær propyl, fra sekundær - sekundær propyl. Feste til det primære eller sekundære kuttet av metyl forårsaker dannelsen av strukturelle varianter av den fjerde homologen. To forbindelser dannes, rettkjedet normal butan og forgrenet isobutan.
Mettede hydrokarboner: struktur
Metan er en typisk representant for alkaner.Molekylformel CH4. Alkanmolekyler er preget av en sigma-binding. I et metanmolekyl danner et karbonatom fire kovalente bindinger på grunn av en s- og tre p-orbitaler, og hvert hydrogenatom - på grunn av en s-orbital.
Mettede hydrokarboner: nomenklatur og isomeri
Når man utleder strukturformlene til det homologeet antall metaner, med utgangspunkt i butan C4H10, møter vi fenomenet isomerisme. For eksempel tilsvarer molekylformelen C4H10 to individuelle forbindelser, C5H12 - tre. Deretter øker antall isomerer med antall karbonatomer i alkanmolekylet. For eksempel tilsvarer molekylformelen C6H14 fem strukturformler og følgelig individuelle stoffer, C7H16 - 9, C8H18 - 18, C10H22 - 76, C12H26 - 355. De første fire representantene for alkaner er gasser, fra den femte til den tolvte - væsker, fra den sekstende - faste stoffer ...
Kjemiske egenskaper til mettede hydrokarboner
Alle mettede hydrokarboner er inerte stoffer.Dette skyldes det faktum at karbon- og hydrogenatomer i alkanmolekyler er bundet av sigma-bindinger, slik at disse forbindelsene ikke kan feste hydrogenatomer. Alkaner inngår i radikale halogenerings-, nitrerings- og spaltingsreaksjoner. I halogeneringsprosessen erstatter halogenatomer lett hydrogenatomer i alkanmolekylet. Under nitrering erstatter nitrogruppen lett hydrogen i tertiær, vanskeligere - i sekundære og primære karbonatomer.
Mettede og umettede hydrokarboner erråvare for å skaffe en rekke organiske stoffer. Ved å dele opp hydrogenatomer fra mettede hydrokarboner, kan umettede (alkener, alkyner) oppnås.