Organska kemija je vrlo složena znanost, alizanimljiv. Uostalom, spojevi istih elemenata, u različitim količinama i slijedovima, doprinose stvaranju tvari različitih svojstava. Pogledajmo spojeve karbonilne skupine zvane "ketoni" (kemijska svojstva, fizikalne karakteristike, metode njihove sinteze). I također ih usporedite s drugim tvarima iste vrste - aldehidima.
Ketoni
Ova riječ je opći naziv za cijelu klasu tvari organske prirode, u čijim je molekulama karbonilna skupina (C = O) povezana s dva ugljikova radikala.
Po svojoj strukturi ketoni su bliski aldehidima i karboksilnim kiselinama. Međutim, oni sadrže dva C atoma odjednom (ugljik ili ugljik) povezana s C = O.

Formula
Opća formula tvari u ovoj klasi je sljedeća: R1-CO-R2.
Da bi bilo razumljivije, u pravilu se ovako piše.

U njemu je C = O karbonilna skupina. A R1 i P2 Jesu li ugljični radikali. Na njihovom mjestu mogu postojati različiti spojevi, ali oni nužno moraju sadržavati ugljik.
Aldehidi i ketoni
Fizikalna i kemijska svojstva ovih skupina tvari prilično su slična jedna drugoj. Iz tog razloga se često promatraju zajedno.
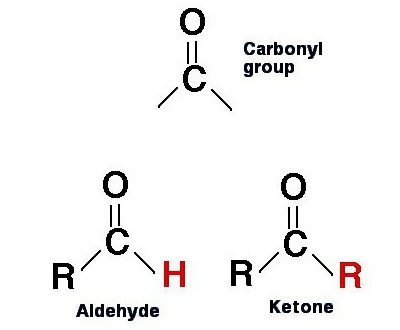
Činjenica je da aldehidi također sadrže u svojimmolekule karbonilne skupine. Čak imaju vrlo slične formule s ketonima. Međutim, ako je u tvarima koje se razmatraju C = O vezan za 2 radikala, onda je u aldehidima samo jedan, umjesto drugog postoji atom vodika: R-CO-H.
Primjer je formula tvari ove klase - formaldehida, svima poznatijeg kao formalin.

Na temelju formule CH2O, može se vidjeti da je njegova karbonilna skupina vezana ne na jedan, već na dva H atoma odjednom.
Fizička svojstva
Prije razumijevanja kemijskih svojstava aldehida i ketona, vrijedno je razmotriti njihove fizičke karakteristike.

- Ketoni su krute tvari ili tekućine niskog taljenja s hlapljivošću. Najniži predstavnici ove klase dobro se otapaju u H2Oko i dobro komunicira s organskim otapalima.
Pojedinačni predstavnici (na primjer, CH3BOR3) izvanredno su topljivi u vodi, i to u apsolutno bilo kojem omjeru.
Za razliku od alkohola i karboksilnih kiselina, ketoniimaju veću hlapljivost, s istom molekulskom težinom. To je olakšano nemogućnošću ovih spojeva da stvore veze s H, kao i H-CO-R. - Različite vrste aldehida mogu biti u različitim agregacijskim stanjima. Dakle, veći R-CO-H su netopive krute tvari. Najmanje su tekućine, od kojih se neke dobro miješaju s H2No, neki od njih su topljivi samo u vodi, ali ne više.
Najjednostavnija tvar ove vrste, mravlji aldehid, je plin oštrog mirisa. Ova tvar je vrlo topiva u H2OKO.
Najpoznatiji ketoni
Postoje mnoge supstance R1-CO-R2, međutim, nije ih toliko poznato. Prije svega, to je dimetil keton, koji svi znamo kao aceton.
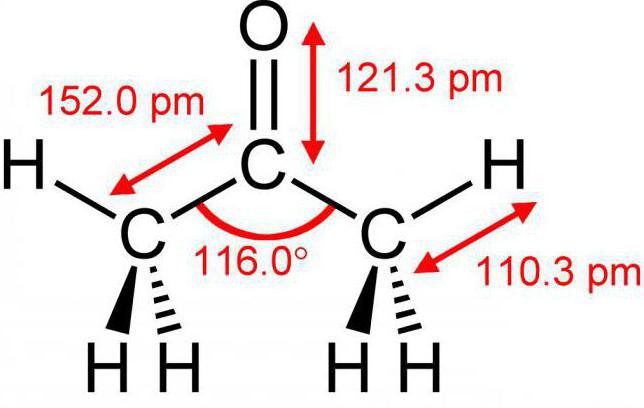
Među ostalim ketonima čija kemijska svojstvaaktivno se koristi u industriji - acetofenon (metil fenil keton). Za razliku od acetona i butanona, njegov je miris prilično ugodan, zbog čega se koristi u parfumeriji.
Na primjer, cikloheksanon pripada tipičnim predstavnicima R1-CO-R2, a najčešće se koristi u proizvodnji otapala.
Nemoguće je ne spomenuti diketone. Ovo je ime R1-CO-R2, koji u svom sastavu imaju ne jednu, već dvije karbonilne skupine. Dakle, njihova formula izgleda ovako: R1-CO-CO-R2... Diacetil (2,3-butandion) je jedan od najjednostavnijih, ali široko korištenih predstavnika diketona u prehrambenoj industriji.
Navedene tvari su samo malopopis ketona koje su sintetizirali znanstvenici (kemijska svojstva su razmotrena u nastavku). Zapravo, ima ih više, ali se ne koriste svi. Štoviše, treba imati na umu da su mnogi od njih otrovni.
Kemijska svojstva ketona
Tvari u ovoj kategoriji sposobne su reagirati s raznim tvarima. Upravo su to njihova posebna kemijska svojstva.
- Ketoni su sposobni vezati H za sebe (reakcijahidrogenacija). Međutim, za proizvodnju ove reakcije neophodna je prisutnost katalizatora u obliku metalnih atoma nikla, kobalta, bakra, platine, paladija i drugih. Kao rezultat reakcije R1-CO-R2 evoluiraju u sekundarne alkohole.
Također, pri interakciji s vodikom u prisutnosti alkalnih metala ili Mg amalgama, iz ketona se dobivaju glikoli. - Ketoni s barem jednimalfa vodikov atom obično je pod utjecajem tautomerizacije ketoenola. Kataliziraju ga ne samo kiseline, već i baze. Obično je keto oblik stabilniji od enolnog oblika. Ova ravnoteža omogućuje sintezu ketona hidratacijom alkina. Relativna stabilizacija enol keto oblika konjugacijom dovodi do prilično jake kiselosti R1-CO-R2 (ako ih usporedite s alkanima).
- Ove tvari mogu reagirati s amonijakom. Međutim, oni napreduju vrlo sporo.
- Ketoni stupaju u interakciju s cijanovodičnom kiselinom. Kao rezultat nastaju α-hidroksinitrili čije saponifikacija doprinosi pojavi α-hidroksi kiselina.
- Reakcija s alkilmagnezij halogenidima dovodi do stvaranja sekundarnih alkohola.
- Pridruživanje NaHSO3 potiče stvaranje hidrosulfitnih (bisulfitnih) derivata. Vrijedno je zapamtiti da samo metil ketoni mogu reagirati u masnom redu.
Osim ketona, aldehidi također mogu djelovati slično s natrijevim hidrosulfitom.
Kada se zagrije s otopinom NaHCO3 (soda bikarbona) ili mineralna kiselina dobivena iz NaHSO3 može se razgraditi, popraćeno oslobađanjem slobodnog ketona. - Tijekom reakcije R1-CO-R2 s NH2Nastaju OH (hidroksilamin) ketoksimi i, kao nusproizvod, H2OKO.
- U reakcijama uz sudjelovanje hidrazina nastaju hidrazoni (omjer uzetih tvari je 1: 1) ili azini (1: 2).
Ako produkt dobiven reakcijom (hidrazon) reagira s kaustičnim kalijem pod utjecajem temperature, oslobodit će se N i zasićeni ugljikovodici. Taj se proces naziva Kizhnerova reakcija. - Kao što je gore spomenuto, aldehidi i ketoni imaju slična kemijska svojstva i proces pripreme. U ovom slučaju, acetali R1-CO-R2 nastaju složeniji od acetala R-CO-H. Pojavljuju se kao rezultat djelovanja na ketone estera ortouraične i ortosilicijeve kiseline.
- U uvjetima s većom koncentracijom lužina (na primjer, pri zagrijavanju koncentriranom H2SO4) R1-CO-R2 podvrgnuti intermolekularnoj dehidraciji s stvaranjem nezasićenih ketona.
- Ako je u reakciji s R1-CO-R2 prisutne su lužine, ketoni podliježu aldolnoj kondenzaciji. Kao rezultat toga nastaju β-keto alkoholi koji lako mogu izgubiti molekulu H2OKO.
- Kemijska svojstva ketona prilično su indikativna za primjer acetona koji je reagirao s mezitil oksidom. U tom slučaju nastaje nova tvar koja se zove foron.
- Također, Leuckart-Wallachova reakcija, koja potiče smanjenje ketona, može se pripisati kemijskim svojstvima dotične organske tvari.
Gdje dobiti R1-CO-R2
Nakon što ste se upoznali sa svojstvima dotičnih tvari, vrijedno je saznati najčešće metode njihove sinteze.
- Jedna od najpoznatijih reakcija za proizvodnju ketona je alkilacija i acilacija aromatskih spojeva u prisutnosti kiselih katalizatora (AlCl3, FeCI3, mineralne kiseline, okside, kationske izmjenjivačke smole itd.). Ova metoda je poznata kao Friedel-Craftsova reakcija.
- Ketoni se sintetiziraju hidrolizom ketimina i vik-diola. U slučaju potonjeg neophodna je prisutnost mineralnih kiselina kao katalizatora.
- Također, za dobivanje ketona koristi se hidratacija homologa acetilena ili, kako se naziva, reakcija Kucherova.
- Guben-Gesh reakcije.
- Ružička ciklizacija je pogodna za sintezu cikloketona.
- Također, ove tvari se ekstrahiraju iz tercijarnih peroksoestera korištenjem Kriegeovog preuređivanja.
- Postoji nekoliko načina za sintezu ketonavrijeme reakcije za oksidaciju sekundarnih alkohola. Ovisno o aktivnom spoju razlikuju se 4 reakcije: Swerna, Kornblum, Kori-Kim i Parik-Dering.
Opseg primjene
Nakon što smo se pozabavili kemijskim svojstvima i proizvodnjom ketona, vrijedi saznati gdje se te tvari koriste.

Kao što je već spomenuto, većina ih se koristi u kemijskoj industriji kao otapala za lakove i emajle, kao i u proizvodnji polimera.
Osim toga, neki R1-CO-R2 dobro su se dokazali kao arome. Kao takvi, ketoni (benzofenon, acetofenon i drugi) se koriste u parfumeriji i kulinarstvu.
Također se acetofenon koristi kao komponenta za proizvodnju tableta za spavanje.

Benzofenon je zbog svoje sposobnosti apsorpcije štetnog zračenja čest sastojak kozmetike protiv tamnjanja, a ujedno i konzervans.
Učinci R1-CO-R2 na tijelo
Učenje koji se spojevi nazivaju ketoni(kemijska svojstva, primjena, sinteza i drugi podaci o njima), vrijedi se upoznati s biološkim karakteristikama ovih tvari. Drugim riječima, saznajte kako djeluju na žive organizme.
Unatoč prilično čestoj upotrebi R1-CO-R2 u industriji, uvijek je vrijedno zapamtiti da su takvi spojevi vrlo otrovni. Mnogi od njih su kancerogeni i mutageni.
Posebni predstavnici mogu izazvati iritaciju na sluznici, sve do opeklina. Aliciklički R1-CO-R2 može utjecati na tijelo poput lijekova.
Međutim, nisu sve tvari ove vrste štetne. Činjenica je da su neki od njih aktivno uključeni u metabolizam bioloških organizama.
Ketoni su također markeri poremećaja metabolizma ugljika i nedostatka inzulina. U analizi urina i krvi, prisutnost R1-CO-R2 ukazuje na različite metaboličke poremećaje, uključujući hiperglikemiju i ketoacidozu.



